ກະວີ:
Lewis Jackson
ວັນທີຂອງການສ້າງ:
12 ເດືອນພຶດສະພາ 2021
ວັນທີປັບປຸງ:
1 ເດືອນກໍລະກົດ 2024
ເນື້ອຫາ
ການ ກຳ ນົດ ຈຳ ນວນນິວຕອນໃນອະຕອມແມ່ນຂ້ອນຂ້າງງ່າຍດາຍ, ທ່ານບໍ່ ຈຳ ເປັນຕ້ອງເຮັດການທົດລອງໃດໆ. ເພື່ອຄິດໄລ່ ຈຳ ນວນນິວເຄຼຍໃນປະລໍາມະນູຫລືໄອໂຊໂທບປົກກະຕິ, ທ່ານພຽງແຕ່ຕ້ອງການໂຕະຕາຕະລາງແຕ່ລະໄລຍະກຽມພ້ອມແລະປະຕິບັດຕາມ ຄຳ ແນະ ນຳ.
ຂັ້ນຕອນ
ວິທີການທີ 1 ຂອງ 2: ຊອກຫາ ຈຳ ນວນຂອງນິວຕອນໃນປະລໍາມະນູ ທຳ ມະດາ
ກຳ ນົດ ຕຳ ແໜ່ງ ຂອງອົງປະກອບໃນຕາຕະລາງແຕ່ລະໄລຍະ. ຍົກຕົວຢ່າງ, ພວກເຮົາຈະພົບເຫັນ osmium (Os) ອົງປະກອບຢູ່ໃນແຖວທີຫົກຈາກດ້ານເທິງ.
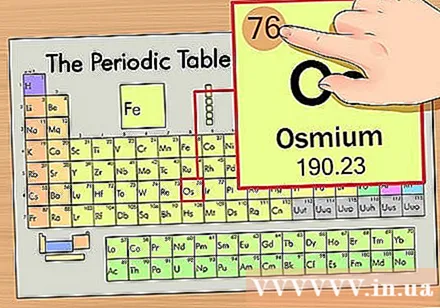
ຊອກຫາຕົວເລກປະລໍາມະນູຂອງອົງປະກອບ. ນີ້ແມ່ນຕົວເລກທີ່ຊັດເຈນທີ່ສຸດທີ່ໄປຕາມແຕ່ລະອົງປະກອບແລະສູງກວ່າສັນຍາລັກທີ່ ສຳ ຄັນ (ຢູ່ເທິງກະດານທີ່ພວກເຮົາ ກຳ ລັງໃຊ້ບໍ່ມີຕົວເລກອື່ນ). ຈໍານວນປະລໍາມະນູແມ່ນຈໍານວນໂປໂຕຄອນໃນປະລໍາມະນູດຽວຂອງທາດນັ້ນ. Os ແມ່ນເລກທີ່ 76, ໝາຍ ຄວາມວ່າມີໂປຣໂຕ 76 ຢູ່ໃນປະລໍາມະນູ osmium.- ຈຳ ນວນໂປໂຕຄອນບໍ່ປ່ຽນແປງໃນອົງປະກອບໃດ ໜຶ່ງ; ມັນເປັນສິ່ງ ຈຳ ເປັນໃນການ ກຳ ນົດລັກສະນະຂອງອົງປະກອບໃດ ໜຶ່ງ.
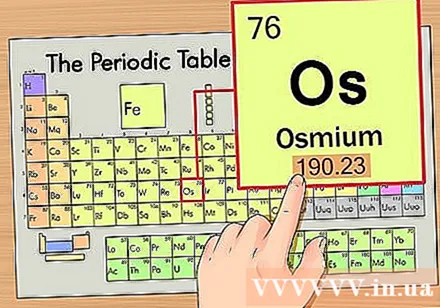
ຊອກຫານໍ້າ ໜັກ ປະລໍາມະນູຂອງອົງປະກອບ. ຕົວເລກນີ້ມັກຈະພົບເຫັນຢູ່ຂ້າງລຸ່ມຂອງເຄື່ອງ ໝາຍ ສຳ ຄັນ. ໃຫ້ສັງເກດວ່າຕາຕະລາງແຕ່ລະໄລຍະໃນຕົວຢ່າງນີ້ມີພຽງແຕ່ຕົວເລກປະລໍາມະນູແລະບໍ່ມີນໍ້າ ໜັກ ປະລໍາມະນູ. ບໍ່ແມ່ນຕາຕະລາງແຕ່ລະໄລຍະ. Osmium ມີນ້ ຳ ໜັກ ປະລໍາມະນູ 190,23.
ຮວບຮວມນ້ ຳ ໜັກ ປະລໍາມະນູໄປຫາເລກເຕັມທີ່ໃກ້ທີ່ສຸດເພື່ອໃຫ້ມວນສານປະລໍາມະນູ. ຍົກຕົວຢ່າງ, 190.23 ຈະເປັນຮູບກົມເຖິງ 190, ສະນັ້ນ, ມະຫາຊົນປະລໍາມະນູຂອງ osmium ແມ່ນ 190.- ນໍ້າ ໜັກ ປະລໍາມະນູແມ່ນມູນຄ່າສະເລ່ຍຂອງ isotopes ຂອງອົງປະກອບເຄມີດຽວກັນ, ຊຶ່ງເປັນເຫດຜົນທີ່ວ່າມັນບໍ່ປົກກະຕິ.
ການຫັກລົບຈໍານວນປະລໍາມະນູຈາກມະຫາຊົນປະລໍາມະນູ. ເນື່ອງຈາກວ່າປະລິມານປະລໍາມະນູສ່ວນໃຫຍ່ແມ່ນທາດໂປຼໂມຊຽມແລະນິວຕອນ, ການຫັກລົບຈໍານວນໂປໂຕຈາກມະຫາປະລໍາມະນູ (ຕົວຢ່າງ: ຈໍານວນປະລໍາມະນູ) ທ່ານ ນັບ ເອົາ ຈຳ ນວນນິວເຄຼຍໃນອະຕອມ. ຕົວເລກຫຼັງຈາກຈຸດທົດສະນິຍົມເປັນຕົວແທນຂອງມວນສານເອເລັກໂຕຣນິກຂະ ໜາດ ນ້ອຍຫຼາຍໃນປະລໍາມະນູ. ໃນຕົວຢ່າງນີ້, ພວກເຮົາມີ: 190 (ອະຕອມຂອງມະຫາຊົນ) - 76 (ຈຳ ນວນໂປໂຕຄອນ) = 114 (ຈຳ ນວນນິວເຄຼຍ).
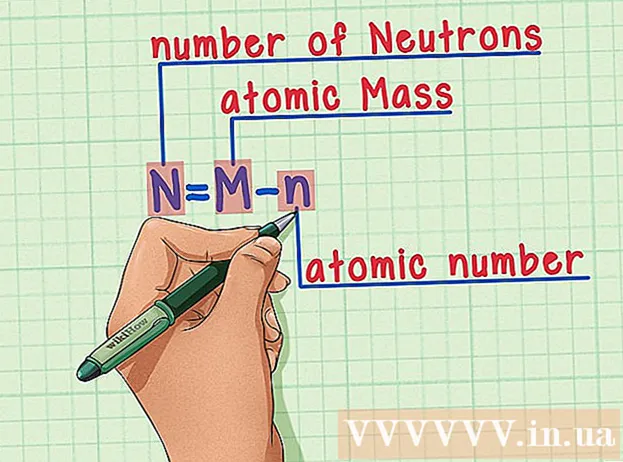
ທ່ອງ ຈຳ ສູດ. ເພື່ອຊອກຫາ ຈຳ ນວນນິວຕອນ, ພວກເຮົາພຽງແຕ່ ນຳ ໃຊ້ສູດດັ່ງຕໍ່ໄປນີ້: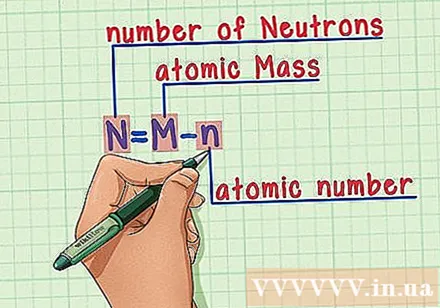
- N = M - ນ
- N = ຈຳ ນວນນິວເຄຼຍ
- M = ມະຫາຊົນປະລໍາມະນູ
- n = ເລກປະລໍາມະນູ
- N = M - ນ
ວິທີທີ່ 2 ຂອງ 2: ຊອກຫາ ຈຳ ນວນຂອງນິວຕອນໃນ isotope
ກຳ ນົດ ຕຳ ແໜ່ງ ຂອງອົງປະກອບໃນຕາຕະລາງແຕ່ລະໄລຍະ. ຂໍໃຫ້ເຮົາພິຈາລະນາທາດ isotope ທາດປະສົມ carbon-14 ເປັນຕົວຢ່າງ. ເນື່ອງຈາກຮູບແບບຂອງ isotope ຂອງກາກບອນ -14 ແມ່ນກາກບອນ (C), ຊອກຫາກາກບອນຢູ່ໃນຕາຕະລາງແຕ່ລະໄລຍະ (ແຖວທີສອງຈາກດ້ານເທິງ).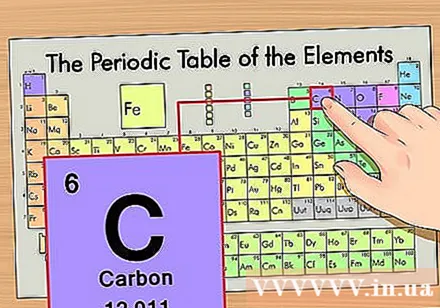
ຊອກຫາຕົວເລກປະລໍາມະນູຂອງອົງປະກອບ. ນີ້ແມ່ນຕົວເລກທີ່ຊັດເຈນທີ່ສຸດທີ່ໄປຕາມແຕ່ລະອົງປະກອບແລະສູງກວ່າສັນຍາລັກທີ່ ສຳ ຄັນ (ຢູ່ເທິງກະດານທີ່ພວກເຮົາ ກຳ ລັງໃຊ້ບໍ່ມີຕົວເລກອື່ນ). ຈໍານວນປະລໍາມະນູແມ່ນຈໍານວນໂປໂຕຄອນໃນປະລໍາມະນູດຽວຂອງທາດນັ້ນ. C ແມ່ນເລກທີ 6, ໝາຍ ຄວາມວ່າມີໂປໂຕຄອນ 6 ໃນອະຕອມຄາບອນ.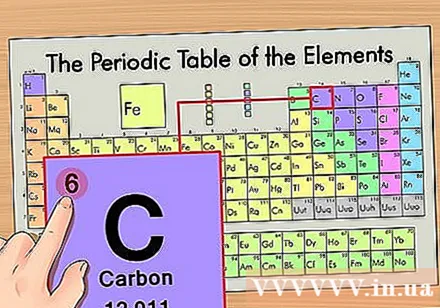
ຊອກຫາມະຫາຊົນປະລໍາມະນູ. ນີ້ແມ່ນງ່າຍທີ່ສຸດກັບ isotopes ເພາະວ່າພວກມັນມີຊື່ຕາມມະຫາປະລໍາມະນູ. ຍົກຕົວຢ່າງ, ກາກບອນ -14 ຈະມີມວນມະຕອມຂອງ 14.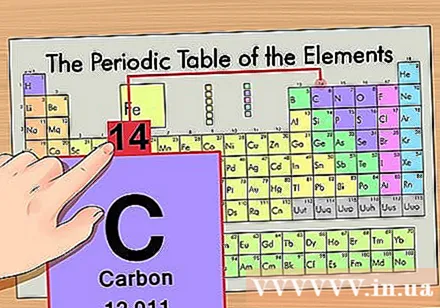
ການຫັກລົບຈໍານວນປະລໍາມະນູຈາກມະຫາຊົນປະລໍາມະນູ. ເນື່ອງຈາກວ່າປະລິມານປະລໍາມະນູສ່ວນໃຫຍ່ແມ່ນທາດໂປຼໂມຊຽມແລະນິວຕອນ, ການຫັກລົບຈໍານວນໂປໂຕຈາກມະຫາປະລໍາມະນູ (ຕົວຢ່າງ: ຈໍານວນປະລໍາມະນູ) ທ່ານ ນັບ ເອົາ ຈຳ ນວນນິວເຄຼຍໃນອະຕອມ. ຕົວເລກຫຼັງຈາກຈຸດທົດສະນິຍົມເປັນຕົວແທນຂອງມວນສານເອເລັກໂຕຣນິກຂະ ໜາດ ນ້ອຍຫຼາຍໃນປະລໍາມະນູ. ໃນຕົວຢ່າງນີ້, ພວກເຮົາມີ: 14 (ອະຕອມຂອງມະຫາຊົນ) - 6 (ຈຳ ນວນໂປໂຕຄອນ) = 8 (ຈຳ ນວນນິວເຄຼຍ).
ທ່ອງ ຈຳ ສູດ. ເພື່ອຊອກຫາ ຈຳ ນວນນິວຕອນ, ພວກເຮົາ ນຳ ໃຊ້ສູດດັ່ງຕໍ່ໄປນີ້: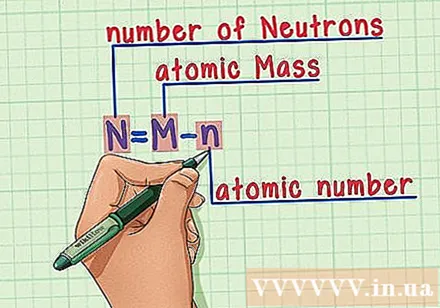
- N = M - ນ
- N = ຈຳ ນວນນິວເຄຼຍ
- M = ມະຫາຊົນປະລໍາມະນູ
- n = ເລກປະລໍາມະນູ
- N = M - ນ
ຄຳ ແນະ ນຳ
- ມະຫາສານຂອງອົງປະກອບສ່ວນໃຫຍ່ແມ່ນມວນສານໂປໂຕຄອນແລະນິວຕອນ, ໃນຂະນະທີ່ມວນສານຂອງອິເລັກໂທຣນິກແລະສ່ວນປະກອບອື່ນໆແມ່ນມີຄວາມລະເລີຍ (ໃກ້ກັບສູນ). ເນື່ອງຈາກວ່າປະລິມານຂອງໂປໂຕຄອນແມ່ນປະມານເທົ່າກັບ ຈຳ ນວນນິວເຄຼຍ, ແລະ ຈຳ ນວນອະຕອມເປັນຕົວແທນ ຈຳ ນວນໂປໂຕຄອນ, ພວກເຮົາພຽງແຕ່ຕ້ອງການຫັກ ຈຳ ນວນໂປໂຕຣຈາກ ຈຳ ນວນມວນທັງ ໝົດ.
- ຖ້າທ່ານບໍ່ຈື່ຄວາມ ໝາຍ ຂອງຕົວເລກໃນຕາຕະລາງແຕ່ລະໄລຍະ, ຈົ່ງ ຈຳ ໄວ້ວ່າຕາຕະລາງແຕ່ລະໄລຍະມັກຈະຖືກສ້າງຂຶ້ນດ້ວຍຕົວເລກປະລໍາມະນູ (ຕົວຢ່າງ ຈຳ ນວນໂປໂຕຄອນ), ເລີ່ມຕົ້ນຈາກ 1 (ໄຮໂດເຈນ) ຊ້າຍຫາຂວາ, ສິ້ນສຸດດ້ວຍ 118 (ununoctium). ເນື່ອງຈາກ ຈຳ ນວນໂປໂຕຄອນແມ່ນຄຸນລັກສະນະທີ່ ກຳ ນົດຂອງແຕ່ລະປະລໍາມະນູ, ມັນແມ່ນຊັບສິນທີ່ລຽບງ່າຍທີ່ສຸດທີ່ອົງປະກອບຈັດລຽງ. (ຍົກຕົວຢ່າງ, ປະລໍາມະນູທີ່ມີ 2 ໂປຣໂຕແມ່ນສະເຫມີຂອງ helium, ຄືກັນກັບອະຕອມທີ່ມີໂປໂຕຄອນ 79 ແມ່ນ ຄຳ ຢູ່ສະ ເໝີ.)
ແຫຼ່ງຂໍ້ມູນແລະການອ້າງອີງ
- ຕາຕະລາງໄລຍະເວລາແບບໂຕ້ຕອບ



