ກະວີ:
Mark Sanchez
ວັນທີຂອງການສ້າງ:
3 ເດືອນມັງກອນ 2021
ວັນທີປັບປຸງ:
1 ເດືອນກໍລະກົດ 2024
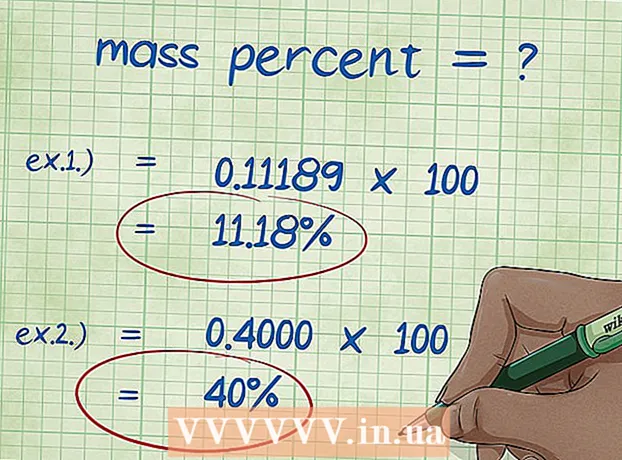
ເນື້ອຫາ
- ຂັ້ນຕອນ
- ວິທີທີ 1 ຂອງ 2: ການກໍານົດເປີເຊັນຂອງມວນສານອີງຕາມນໍ້າ ໜັກ ທີ່ລະບຸ
- ວິທີທີ່ 2 ຂອງ 2: ການກໍານົດເປີເຊັນຂອງມວນເມື່ອບໍ່ມີການລະບຸຈໍານວນມະຫາຊົນ
ເປີເຊັນຂອງມະຫາຊົນລະບຸເປີເຊັນຂອງອົງປະກອບໃນສານເຄມີປະສົມ. ເພື່ອຊອກຫາອັດຕາສ່ວນຂອງມວນ, ເຈົ້າຕ້ອງຮູ້ຈັກມວນສານໂມເລກຸນ (ເປັນກຼາມຕໍ່ໂມເລກຸນ) ຂອງອົງປະກອບທີ່ລວມຢູ່ໃນສານປະກອບຫຼືຈໍານວນກຼາມຂອງແຕ່ລະສ່ວນປະກອບທີ່ຕ້ອງການເພື່ອໃຫ້ໄດ້ຄໍາຕອບທີ່ໄດ້ຮັບມາ.ອັດຕາສ່ວນຂອງມະຫາຊົນໄດ້ຖືກຄິດໄລ່ຂ້ອນຂ້າງງ່າຍ: ມັນພຽງພໍທີ່ຈະແບ່ງມວນຂອງອົງປະກອບ (ຫຼືສ່ວນປະກອບ) ໂດຍມວນຂອງທາດປະສົມທັງ(ົດ (ຫຼືການແກ້ໄຂ).
ຂັ້ນຕອນ
ວິທີທີ 1 ຂອງ 2: ການກໍານົດເປີເຊັນຂອງມວນສານອີງຕາມນໍ້າ ໜັກ ທີ່ລະບຸ
 1 ເລືອກສົມຜົນເພື່ອກໍານົດອັດຕາສ່ວນນໍ້າ ໜັກ ຂອງທາດປະສົມເຄມີ. ເປີເຊັນຂອງມວນສານແມ່ນ ຄຳ ນວນໂດຍໃຊ້ສູດຕໍ່ໄປນີ້: ອັດຕາສ່ວນຂອງມວນ = (ມວນຂອງສ່ວນປະກອບ / ມວນສານປະກອບທັງ)ົດ) x 100. ເພື່ອໃຫ້ໄດ້ເປີເຊັນ, ຜົນຂອງການຫານແມ່ນຄູນດ້ວຍ 100.
1 ເລືອກສົມຜົນເພື່ອກໍານົດອັດຕາສ່ວນນໍ້າ ໜັກ ຂອງທາດປະສົມເຄມີ. ເປີເຊັນຂອງມວນສານແມ່ນ ຄຳ ນວນໂດຍໃຊ້ສູດຕໍ່ໄປນີ້: ອັດຕາສ່ວນຂອງມວນ = (ມວນຂອງສ່ວນປະກອບ / ມວນສານປະກອບທັງ)ົດ) x 100. ເພື່ອໃຫ້ໄດ້ເປີເຊັນ, ຜົນຂອງການຫານແມ່ນຄູນດ້ວຍ 100. - ໃນຕອນເລີ່ມຕົ້ນຂອງການແກ້ໄຂບັນຫາ, ໃຫ້ຂຽນຄວາມເທົ່າທຽມກັນໄວ້: ເປີເຊັນຂອງມວນ = (ມວນຂອງສ່ວນປະກອບ / ມວນສານທັງofົດ) x 100.
- ມະຫາຊົນຂອງອົງປະກອບທີ່ເຈົ້າສົນໃຈຄວນຢູ່ໃນສະພາບຂອງບັນຫາ. ຖ້າບໍ່ມີການໃຫ້ມວນສານ, ໃຫ້ຂ້າມໄປຫາພາກຕໍ່ໄປ, ເຊິ່ງອະທິບາຍວິທີການກໍານົດອັດຕາສ່ວນຂອງມວນດ້ວຍມວນທີ່ບໍ່ຮູ້ຈັກ.
- ມວນສານເຄມີທັງisົດແມ່ນພົບໄດ້ໂດຍການເພີ່ມມວນຂອງທຸກ elements ອົງປະກອບ (ສ່ວນປະກອບ) ທີ່ເປັນສ່ວນ ໜຶ່ງ ຂອງສານປະສົມນີ້ (ຫຼືທາດລະລາຍ).
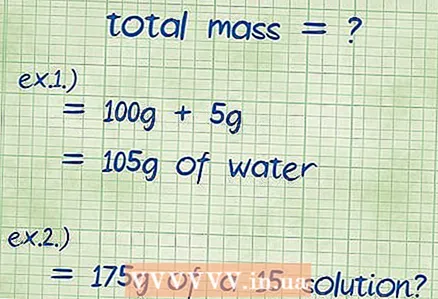 2 ຄິດໄລ່ມວນສານທັງົດຂອງທາດປະສົມ. ຖ້າເຈົ້າຮູ້ຈັກມະຫາຊົນຂອງສ່ວນປະກອບທັງthatົດທີ່ປະກອບເປັນທາດປະສົມ, ພຽງແຕ່ເພີ່ມພວກມັນເຂົ້າກັນ, ແລະວິທີນີ້ເຈົ້າຈະພົບເຫັນມວນລວມຂອງການປະສົມຫຼືການແກ້ໄຂບັນຫາ. ເຈົ້າໃຊ້ມະຫາຊົນນີ້ເປັນຕົວຫານໃນສົມຜົນຂອງເຈົ້າເປັນເປີເຊັນຂອງມວນ.
2 ຄິດໄລ່ມວນສານທັງົດຂອງທາດປະສົມ. ຖ້າເຈົ້າຮູ້ຈັກມະຫາຊົນຂອງສ່ວນປະກອບທັງthatົດທີ່ປະກອບເປັນທາດປະສົມ, ພຽງແຕ່ເພີ່ມພວກມັນເຂົ້າກັນ, ແລະວິທີນີ້ເຈົ້າຈະພົບເຫັນມວນລວມຂອງການປະສົມຫຼືການແກ້ໄຂບັນຫາ. ເຈົ້າໃຊ້ມະຫາຊົນນີ້ເປັນຕົວຫານໃນສົມຜົນຂອງເຈົ້າເປັນເປີເຊັນຂອງມວນ. - ຕົວຢ່າງ 1: ອັດຕາສ່ວນມວນສານ 5 ກຼາມຂອງໂຊດຽມໄຮໂດຣໄຊດ dissol ທີ່ລະລາຍຢູ່ໃນນໍ້າ 100 ກຣາມແມ່ນເທົ່າໃດ?
- ມວນສານທັງofົດຂອງການແກ້ບັນຫາແມ່ນເທົ່າກັບຜົນລວມຂອງປະລິມານໂຊດຽມໄຮໂດຣໄຊແລະນໍ້າ: 100 g + 5 g ໃຫ້ 105 g.
- ຕົວຢ່າງ 2: ເຈົ້າຕ້ອງການນໍ້າໂຊດຽມຄລໍໄຣແລະນໍ້າຫຼາຍປານໃດເພື່ອເຮັດ 175 ກຣາມຂອງວິທີແກ້ໄຂ 15 ເປີເຊັນ?
- ໃນຕົວຢ່າງນີ້, ໃຫ້ປະລິມານທັງandົດແລະເປີເຊັນທີ່ຕ້ອງການ, ແລະມັນ ຈຳ ເປັນຕ້ອງຊອກຫາປະລິມານຂອງສານທີ່ຕ້ອງການເພີ່ມເຂົ້າໄປໃນການແກ້ໄຂ. ນ້ ຳ ໜັກ ລວມແມ່ນ 175 ກຼາມ.
- ຕົວຢ່າງ 1: ອັດຕາສ່ວນມວນສານ 5 ກຼາມຂອງໂຊດຽມໄຮໂດຣໄຊດ dissol ທີ່ລະລາຍຢູ່ໃນນໍ້າ 100 ກຣາມແມ່ນເທົ່າໃດ?
 3 ກໍານົດມະຫາຊົນຂອງອົງປະກອບທີ່ລະບຸ. ຖ້າເຈົ້າຖືກຖາມໃຫ້ຄິດໄລ່ "ເປີເຊັນຂອງມວນ", ເຈົ້າຄວນຊອກຫາວ່າເປີເຊັນຂອງມວນສານທັງisົດແມ່ນມວນຂອງສ່ວນປະກອບໃດນຶ່ງ. ບັນທຶກມວນສານຂອງສ່ວນປະກອບທີ່ລະບຸ. ອັນນີ້ຈະເປັນຕົວເສດໃນສູດຄິດໄລ່ເປີເຊັນຂອງມວນສານ.
3 ກໍານົດມະຫາຊົນຂອງອົງປະກອບທີ່ລະບຸ. ຖ້າເຈົ້າຖືກຖາມໃຫ້ຄິດໄລ່ "ເປີເຊັນຂອງມວນ", ເຈົ້າຄວນຊອກຫາວ່າເປີເຊັນຂອງມວນສານທັງisົດແມ່ນມວນຂອງສ່ວນປະກອບໃດນຶ່ງ. ບັນທຶກມວນສານຂອງສ່ວນປະກອບທີ່ລະບຸ. ອັນນີ້ຈະເປັນຕົວເສດໃນສູດຄິດໄລ່ເປີເຊັນຂອງມວນສານ. - ຕົວຢ່າງ 1: ມວນສານຂອງສ່ວນປະກອບທີ່ໃຫ້ມາ - sodium hydrochloride - ແມ່ນ 5 ກຣາມ.
- ຕົວຢ່າງ 2: ໃນຕົວຢ່າງນີ້, ມວນສານຂອງອົງປະກອບທີ່ໃຫ້ແມ່ນບໍ່ຮູ້ຈັກແລະຕ້ອງໄດ້ພົບເຫັນ.
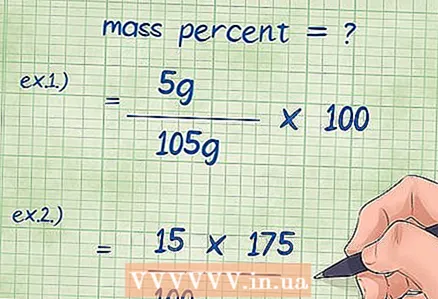 4 ສຽບຄ່າເຂົ້າໄປໃນສົມຜົນເປີເຊັນມະຫາຊົນ. ຫຼັງຈາກທີ່ເຈົ້າໄດ້ ກຳ ນົດຄ່າທັງrequiredົດທີ່ຕ້ອງການ, ສຽບພວກມັນເຂົ້າໄປໃນສູດ.
4 ສຽບຄ່າເຂົ້າໄປໃນສົມຜົນເປີເຊັນມະຫາຊົນ. ຫຼັງຈາກທີ່ເຈົ້າໄດ້ ກຳ ນົດຄ່າທັງrequiredົດທີ່ຕ້ອງການ, ສຽບພວກມັນເຂົ້າໄປໃນສູດ. - ຕົວຢ່າງ 1: ເປີເຊັນຂອງມະຫາຊົນ = (ມວນສານຂອງສ່ວນປະກອບ / ມວນສານທັງofົດ) x 100 = (5 g / 105 g) x 100.
- ຕົວຢ່າງ 2: ມັນຈໍາເປັນຕ້ອງປ່ຽນສູດສໍາລັບເປີເຊັນຂອງມວນສານເພື່ອໃຫ້ມວນສານເຄມີທີ່ບໍ່ຮູ້ຈັກສາມາດພົບໄດ້: ມວນຂອງສ່ວນປະກອບ = (ເປີເຊັນຂອງມະຫາຊົນ * ມວນສານທັງofົດຂອງທາດປະສົມ) / 100 = (15 *) 175) / 100.
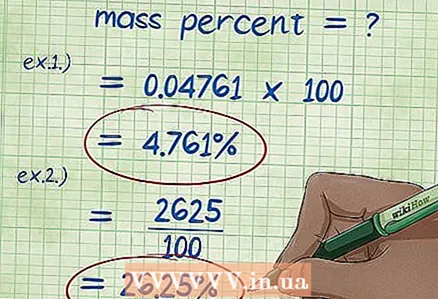 5 ຄິດໄລ່ອັດຕາສ່ວນມະຫາຊົນ. ຫຼັງຈາກແທນຄ່າທັງinົດໃນສູດ ສຳ ລັບເປີເຊັນມະຫາຊົນ, ໃຫ້ເຮັດການຄິດໄລ່ທີ່ ຈຳ ເປັນ. ຫານມະຫາຊົນຂອງອົງປະກອບ ໜຶ່ງ ໂດຍນໍ້າ ໜັກ ທັງົດຂອງທາດປະສົມເຄມີຫຼືການແກ້ໄຂບັນຫາແລະຄູນດ້ວຍ 100. ຜົນໄດ້ຮັບແມ່ນເປີເຊັນມະຫາຊົນຂອງສ່ວນປະກອບນັ້ນ.
5 ຄິດໄລ່ອັດຕາສ່ວນມະຫາຊົນ. ຫຼັງຈາກແທນຄ່າທັງinົດໃນສູດ ສຳ ລັບເປີເຊັນມະຫາຊົນ, ໃຫ້ເຮັດການຄິດໄລ່ທີ່ ຈຳ ເປັນ. ຫານມະຫາຊົນຂອງອົງປະກອບ ໜຶ່ງ ໂດຍນໍ້າ ໜັກ ທັງົດຂອງທາດປະສົມເຄມີຫຼືການແກ້ໄຂບັນຫາແລະຄູນດ້ວຍ 100. ຜົນໄດ້ຮັບແມ່ນເປີເຊັນມະຫາຊົນຂອງສ່ວນປະກອບນັ້ນ. - ຕົວຢ່າງ 1: (5/105) x 100 = 0.04761 x 100 = 4.761%. ດັ່ງນັ້ນ, ອັດຕາສ່ວນນໍ້າ ໜັກ ຂອງ 5 ກຼາມຂອງໂຊດຽມໄຮໂດຄລໍໄຣທີ່ລະລາຍຢູ່ໃນນໍ້າ 100 ກຣາມແມ່ນ 4.761%.
- ຕົວຢ່າງ 2: ການສະແດງອອກທີ່ຂຽນຄືນໃpercentage່ສໍາລັບເປີເຊັນມວນຂອງອົງປະກອບແມ່ນ (ເປີເຊັນຂອງມະຫາຊົນ * ມວນສານທັງofົດຂອງສານ) / 100, ຈາກທີ່ພວກເຮົາພົບ: (15 * 175) / 100 = (2625) / 100 = 26.25 ກຣາມ ຂອງ sodium chloride.
- ພວກເຮົາຊອກຫາປະລິມານນໍ້າທີ່ຕ້ອງການໂດຍການຫັກລົບເອົາມວນຂອງອົງປະກອບອອກຈາກມວນນໍ້າທັງofົດຂອງການແກ້ໄຂ: 175 - 26.25 = 148.75 ກຣາມຂອງນໍ້າ.
ວິທີທີ່ 2 ຂອງ 2: ການກໍານົດເປີເຊັນຂອງມວນເມື່ອບໍ່ມີການລະບຸຈໍານວນມະຫາຊົນ
 1 ເລືອກສູດສໍາລັບເປີເຊັນນໍ້າ ໜັກ ຂອງທາດປະສົມເຄມີ. ສົມຜົນພື້ນຖານສໍາລັບການຊອກຫາເປີເຊັນຂອງມວນສານມີດັ່ງນີ້: ເປີເຊັນຂອງມວນ = (ມວນໂມເລກຸນຂອງອົງປະກອບ / ມວນສານໂມເລກຸນທັງofົດຂອງທາດປະສົມ) x 100. ມວນສານໂມເລກຸນຂອງສານແມ່ນມວນສານຂອງໂມເລກຸນ ໜຶ່ງ ຂອງສານທີ່ໄດ້ຮັບ, ໃນຂະນະທີ່ມະຫາຊົນໂມເລກຸນ ແມ່ນມະຫາຊົນຂອງໂມເລກຸນ ໜຶ່ງ ຂອງການເຊື່ອມຕໍ່ທາງເຄມີທັງົດ. ການຫານແມ່ນຄູນດ້ວຍ 100 ເພື່ອໃຫ້ໄດ້ເປີເຊັນ.
1 ເລືອກສູດສໍາລັບເປີເຊັນນໍ້າ ໜັກ ຂອງທາດປະສົມເຄມີ. ສົມຜົນພື້ນຖານສໍາລັບການຊອກຫາເປີເຊັນຂອງມວນສານມີດັ່ງນີ້: ເປີເຊັນຂອງມວນ = (ມວນໂມເລກຸນຂອງອົງປະກອບ / ມວນສານໂມເລກຸນທັງofົດຂອງທາດປະສົມ) x 100. ມວນສານໂມເລກຸນຂອງສານແມ່ນມວນສານຂອງໂມເລກຸນ ໜຶ່ງ ຂອງສານທີ່ໄດ້ຮັບ, ໃນຂະນະທີ່ມະຫາຊົນໂມເລກຸນ ແມ່ນມະຫາຊົນຂອງໂມເລກຸນ ໜຶ່ງ ຂອງການເຊື່ອມຕໍ່ທາງເຄມີທັງົດ. ການຫານແມ່ນຄູນດ້ວຍ 100 ເພື່ອໃຫ້ໄດ້ເປີເຊັນ. - ໃນຕອນເລີ່ມຕົ້ນຂອງການແກ້ໄຂບັນຫາ, ໃຫ້ຂຽນຄວາມເທົ່າທຽມກັນໄວ້: ເປີເຊັນຂອງມວນ = (ມວນໂມເລກຸນຂອງອົງປະກອບ / ມວນສານໂມເລກຸນທັງofົດຂອງທາດປະສົມ) x 100.
- ປະລິມານທັງສອງຖືກວັດແທກເປັນກຼາມຕໍ່ໂມເລກຸນ (g / mol).
- ຖ້າເຈົ້າບໍ່ໄດ້ໃຫ້ມວນສານ, ອັດຕາສ່ວນມວນຂອງອົງປະກອບຢູ່ໃນສານທີ່ໃຫ້ມາສາມາດພົບໄດ້ໂດຍການໃຊ້ມວນສານໂມນ.
- ຕົວຢ່າງ 1: ຊອກຫາອັດຕາສ່ວນຂອງ hydrogen ໃນໂມເລກຸນຂອງນໍ້າ.
- ຕົວຢ່າງ 2: ຊອກຫາອັດຕາສ່ວນຂອງກາກບອນໃນໂມເລກຸນທາດນ້ ຳ ຕານ.
 2 ຂຽນສູດເຄມີ. ຖ້າຕົວຢ່າງບໍ່ໄດ້ໃຫ້ສູດເຄມີຂອງສານທີ່ລະບຸ, ເຈົ້າຄວນຂຽນມັນລົງດ້ວຍຕົວເຈົ້າເອງ. ຖ້າ ໜ້າ ວຽກມີສູດທີ່ຈໍາເປັນສໍາລັບສານເຄມີ, ເຈົ້າສາມາດຂ້າມຂັ້ນຕອນນີ້ແລະໄປຫາຂັ້ນຕອນຕໍ່ໄປໂດຍກົງ (ຊອກຫາມວນຂອງແຕ່ລະອົງປະກອບ).
2 ຂຽນສູດເຄມີ. ຖ້າຕົວຢ່າງບໍ່ໄດ້ໃຫ້ສູດເຄມີຂອງສານທີ່ລະບຸ, ເຈົ້າຄວນຂຽນມັນລົງດ້ວຍຕົວເຈົ້າເອງ. ຖ້າ ໜ້າ ວຽກມີສູດທີ່ຈໍາເປັນສໍາລັບສານເຄມີ, ເຈົ້າສາມາດຂ້າມຂັ້ນຕອນນີ້ແລະໄປຫາຂັ້ນຕອນຕໍ່ໄປໂດຍກົງ (ຊອກຫາມວນຂອງແຕ່ລະອົງປະກອບ). - ຕົວຢ່າງ 1: ຂຽນສູດເຄມີຂອງນໍ້າ, H2ໂອ.
- ຕົວຢ່າງ 2: ຂຽນສູດເຄມີຂອງນ້ ຳ ຕານ, C6ຮ12ໂອ6.
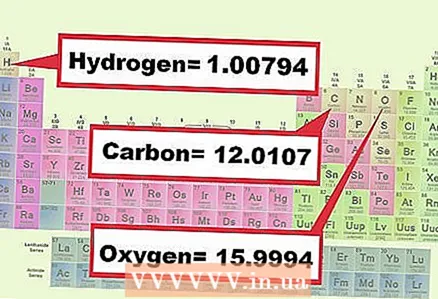 3 ຊອກຫາມວນສານຂອງແຕ່ລະອົງປະກອບໃນທາດປະສົມ. ກຳ ນົດນ້ ຳ ໜັກ ໂມເລກຸນຂອງແຕ່ລະອົງປະກອບໃນສູດເຄມີຕາມຕາຕະລາງແຕ່ລະໄລຍະ. ໂດຍປົກກະຕິ, ມວນສານຂອງອົງປະກອບໃດ ໜຶ່ງ ຈະຖືກຊີ້ບອກພາຍໃຕ້ສັນຍາລັກທາງເຄມີຂອງມັນ. ຂຽນປະລິມານ molar ຂອງອົງປະກອບທັງthatົດທີ່ປະກອບເປັນທາດປະສົມໃນຄໍາຖາມ.
3 ຊອກຫາມວນສານຂອງແຕ່ລະອົງປະກອບໃນທາດປະສົມ. ກຳ ນົດນ້ ຳ ໜັກ ໂມເລກຸນຂອງແຕ່ລະອົງປະກອບໃນສູດເຄມີຕາມຕາຕະລາງແຕ່ລະໄລຍະ. ໂດຍປົກກະຕິ, ມວນສານຂອງອົງປະກອບໃດ ໜຶ່ງ ຈະຖືກຊີ້ບອກພາຍໃຕ້ສັນຍາລັກທາງເຄມີຂອງມັນ. ຂຽນປະລິມານ molar ຂອງອົງປະກອບທັງthatົດທີ່ປະກອບເປັນທາດປະສົມໃນຄໍາຖາມ. - ຕົວຢ່າງ 1: ຊອກຫາອົກຊີແຊນໂມເລກຸນ (15.9994) ແລະໄຮໂດເຈນ (1.0079).
- ຕົວຢ່າງ 2: ຊອກຫາທາດໂມເລກຸນຄາບອນ (12.0107), ອົກຊີ (15.9994) ແລະໄຮໂດເຈນ (1.0079).
 4 ຄູນມວນມະຫາຊົນຂອງແຕ່ລະອົງປະກອບດ້ວຍສ່ວນປະກອບຂອງມັນທີ່ເປັນໂມຄະ. ກວດເບິ່ງວ່າມີຈັກໂມເລກຸນຂອງແຕ່ລະອົງປະກອບທີ່ບັນຈຸຢູ່ໃນສານເຄມີທີ່ໄດ້ຮັບ, ນັ້ນແມ່ນ, ສ່ວນປະກອບຂອງໂມເລກຸນຂອງອົງປະກອບ. ເສດສ່ວນຂອງໂມເລກຸນແມ່ນໃຫ້ໂດຍຕົວເລກຢູ່ທາງລຸ່ມຂອງສັນຍາລັກອົງປະກອບໃນສູດ. ຄູນມວນມະຫາຊົນຂອງແຕ່ລະອົງປະກອບດ້ວຍສ່ວນປະກອບຂອງມັນທີ່ເປັນໂມຄະ.
4 ຄູນມວນມະຫາຊົນຂອງແຕ່ລະອົງປະກອບດ້ວຍສ່ວນປະກອບຂອງມັນທີ່ເປັນໂມຄະ. ກວດເບິ່ງວ່າມີຈັກໂມເລກຸນຂອງແຕ່ລະອົງປະກອບທີ່ບັນຈຸຢູ່ໃນສານເຄມີທີ່ໄດ້ຮັບ, ນັ້ນແມ່ນ, ສ່ວນປະກອບຂອງໂມເລກຸນຂອງອົງປະກອບ. ເສດສ່ວນຂອງໂມເລກຸນແມ່ນໃຫ້ໂດຍຕົວເລກຢູ່ທາງລຸ່ມຂອງສັນຍາລັກອົງປະກອບໃນສູດ. ຄູນມວນມະຫາຊົນຂອງແຕ່ລະອົງປະກອບດ້ວຍສ່ວນປະກອບຂອງມັນທີ່ເປັນໂມຄະ. - ຕົວຢ່າງ 1: ມີ 2 ພາຍໃຕ້ສັນຍາລັກໄຮໂດເຈນ, ແລະ 1 ຕົວຢູ່ພາຍໃຕ້ສັນຍາລັກຂອງອົກຊີ (ທຽບເທົ່າກັບບໍ່ມີຕົວເລກ). ດັ່ງນັ້ນ, ມວນສານໂມເລກຸນຂອງ hydrogen ຄວນຄູນດ້ວຍ 2: 1.00794 X 2 = 2.01588; ພວກເຮົາປ່ອຍໃຫ້ອົກຊີໃນມວນໂມເລກຸນເທົ່າກັນ, 15.9994 (ນັ້ນຄື, ຄູນດ້ວຍ 1).
- ຕົວຢ່າງ 2: ພາຍໃຕ້ສັນຍາລັກຂອງກາກບອນມີ 6, ຢູ່ໃຕ້ນໍ້າໄຮໂດເຈນ 12 ແລະພາຍໃຕ້ອົກຊີແຊນ 6. ຄູນມວນມະຫາຊົນຂອງໂມເລກຸນດ້ວຍຕົວເລກເຫຼົ່ານີ້, ພວກເຮົາພົບວ່າ:
- ຄາບອນ: (12.0107 * 6) = 72.0642
- ໄຮໂດເຈນ: (1.00794 * 12) = 12.09528
- ອົກຊີເຈນ: (15.9994 * 6) = 95.9964
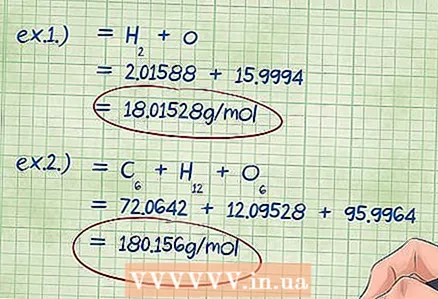 5 ຄິດໄລ່ມວນສານທັງົດຂອງທາດປະສົມ. ເພີ່ມມະຫາຊົນທີ່ພົບເຫັນຂອງອົງປະກອບທັງincludedົດທີ່ລວມຢູ່ໃນສານປະສົມນີ້. ຜົນລວມຂອງມະຫາຊົນ molar ຂອງອົງປະກອບຄູນດ້ວຍສ່ວນປະກອບຂອງໂມເລກຸນຈະເຮັດໃຫ້ເຈົ້າມີມວນສານປະສົມສານເຄມີທັງyouົດ. ຕົວເລກນີ້ແມ່ນຕົວຫານໃນສູດຂອງເປີເຊັນມະຫາຊົນ.
5 ຄິດໄລ່ມວນສານທັງົດຂອງທາດປະສົມ. ເພີ່ມມະຫາຊົນທີ່ພົບເຫັນຂອງອົງປະກອບທັງincludedົດທີ່ລວມຢູ່ໃນສານປະສົມນີ້. ຜົນລວມຂອງມະຫາຊົນ molar ຂອງອົງປະກອບຄູນດ້ວຍສ່ວນປະກອບຂອງໂມເລກຸນຈະເຮັດໃຫ້ເຈົ້າມີມວນສານປະສົມສານເຄມີທັງyouົດ. ຕົວເລກນີ້ແມ່ນຕົວຫານໃນສູດຂອງເປີເຊັນມະຫາຊົນ. - ຕົວຢ່າງ 1: ເພີ່ມເຂົ້າໄປໃນ 2.01588 g / mol (ມະຫາຊົນຂອງສອງໂມເລກຸນຂອງອະຕອມໄຮໂດເຈນ) 15.9994 g / mol (ມວນ ໜຶ່ງ ຂອງໂມເລກຸນຂອງປະລໍາມະນູອົກຊີ), ຜົນໄດ້ຮັບແມ່ນ 18.01528 g / mol.
- ຕົວຢ່າງ 2: ເພີ່ມມວນສານໂມເລກຸນທີ່ພົບ: ຄາບອນ + ໄຮໂດເຈນ + ອົກຊີ = 72.0642 + 12.09528 + 95.9964 = 180.156 g / mol.
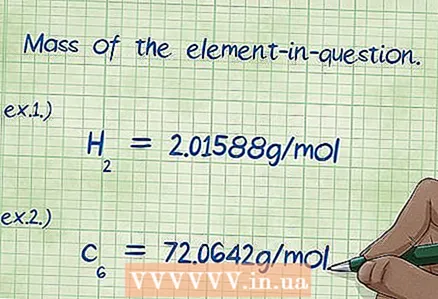 6 ກໍານົດມະຫາຊົນຂອງອົງປະກອບທີ່ສົນໃຈ. ຖ້າເຈົ້າຖືກຖາມໃຫ້ຊອກຫາ "ເປີເຊັນຂອງມວນ", ຈາກນັ້ນເຈົ້າຄວນ ຄຳ ນວນມວນສານຂອງອົງປະກອບໃດ ໜຶ່ງ ທີ່ເປັນສ່ວນ ໜຶ່ງ ຂອງສານປະກອບ, ເປັນເປີເຊັນຂອງມວນລວມທັງofົດຂອງທຸກອົງປະກອບ. ຊອກຫາມວນສານຂອງອົງປະກອບທີ່ໃຫ້ມາແລະຂຽນມັນລົງ. ເພື່ອເຮັດສິ່ງນີ້, ມັນເປັນສິ່ງ ຈຳ ເປັນທີ່ຈະຕ້ອງຄູນມວນໂມເລກຸນຂອງສ່ວນປະກອບດ້ວຍສ່ວນປະກອບຂອງມັນ. ຜົນກໍຄື, ເຈົ້າໄດ້ຮັບຄ່າໃນຕົວເສດຂອງສູດຄິດໄລ່ເປີເຊັນຂອງມວນສານ.
6 ກໍານົດມະຫາຊົນຂອງອົງປະກອບທີ່ສົນໃຈ. ຖ້າເຈົ້າຖືກຖາມໃຫ້ຊອກຫາ "ເປີເຊັນຂອງມວນ", ຈາກນັ້ນເຈົ້າຄວນ ຄຳ ນວນມວນສານຂອງອົງປະກອບໃດ ໜຶ່ງ ທີ່ເປັນສ່ວນ ໜຶ່ງ ຂອງສານປະກອບ, ເປັນເປີເຊັນຂອງມວນລວມທັງofົດຂອງທຸກອົງປະກອບ. ຊອກຫາມວນສານຂອງອົງປະກອບທີ່ໃຫ້ມາແລະຂຽນມັນລົງ. ເພື່ອເຮັດສິ່ງນີ້, ມັນເປັນສິ່ງ ຈຳ ເປັນທີ່ຈະຕ້ອງຄູນມວນໂມເລກຸນຂອງສ່ວນປະກອບດ້ວຍສ່ວນປະກອບຂອງມັນ. ຜົນກໍຄື, ເຈົ້າໄດ້ຮັບຄ່າໃນຕົວເສດຂອງສູດຄິດໄລ່ເປີເຊັນຂອງມວນສານ. - ຕົວຢ່າງ 1: ມວນສານຂອງໄຮໂດເຈນໃນທາດປະສົມແມ່ນ 2.01588 g / mol (ມວນຂອງໂມເລກຸນອະຕອມໄຮໂດຣເຈນສອງໂມເລກຸນ).
- ຕົວຢ່າງ 2: ມວນຄາບອນໃນທາດປະສົມແມ່ນ 72.0642 g / mol (ມວນຂອງອະຕອມຄາບອນ 6 ໂມເລກຸນ).
 7 ແທນຄ່າຂອງຕົວເລກເຂົ້າໄປໃນສົມຜົນເປີເຊັນມະຫາຊົນ. ຫຼັງຈາກທີ່ເຈົ້າກໍານົດຄຸນຄ່າຂອງປະລິມານທັງ,ົດ, ສຽບພວກມັນເຂົ້າໄປໃນສູດທີ່ໄດ້ໃຫ້ໄວ້ໃນຂັ້ນຕອນທໍາອິດ: ອັດຕາສ່ວນຂອງມວນ = (ມວນໂມເລກຸນຂອງອົງປະກອບ / ມວນໂມເລກຸນທັງofົດຂອງທາດປະສົມ) x 100.
7 ແທນຄ່າຂອງຕົວເລກເຂົ້າໄປໃນສົມຜົນເປີເຊັນມະຫາຊົນ. ຫຼັງຈາກທີ່ເຈົ້າກໍານົດຄຸນຄ່າຂອງປະລິມານທັງ,ົດ, ສຽບພວກມັນເຂົ້າໄປໃນສູດທີ່ໄດ້ໃຫ້ໄວ້ໃນຂັ້ນຕອນທໍາອິດ: ອັດຕາສ່ວນຂອງມວນ = (ມວນໂມເລກຸນຂອງອົງປະກອບ / ມວນໂມເລກຸນທັງofົດຂອງທາດປະສົມ) x 100. - ຕົວຢ່າງ 1: ເປີເຊັນຂອງມະຫາຊົນ = (ມວນສານໂມເລກຸນຂອງທາດ / ປະລິມານໂມເລກຸນທັງofົດຂອງທາດປະສົມ) x 100 = (2.01588 / 18.01528) x 100.
- ຕົວຢ່າງ 2: ເປີເຊັນຂອງມະຫາຊົນ = (ມວນໂມເລກຸນຂອງອົງປະກອບ / ມວນສານໂມເລກຸນທັງofົດຂອງທາດປະສົມ) x 100 = (72.0642 / 180.156) x 100.
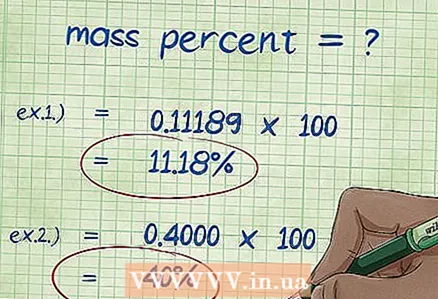 8 ຄິດໄລ່ອັດຕາສ່ວນມະຫາຊົນ. ຫຼັງຈາກການປ່ຽນແທນຄ່າຕົວເລກ, ໃຫ້ດໍາເນີນການດໍາເນີນຄະນິດສາດທີ່ຕ້ອງການ.ຫານມວນຂອງອົງປະກອບດ້ວຍມວນທັງofົດຂອງທາດປະສົມແລະຄູນດ້ວຍ 100. ຜົນໄດ້ຮັບແມ່ນເປີເຊັນມະຫາຊົນຂອງທາດ.
8 ຄິດໄລ່ອັດຕາສ່ວນມະຫາຊົນ. ຫຼັງຈາກການປ່ຽນແທນຄ່າຕົວເລກ, ໃຫ້ດໍາເນີນການດໍາເນີນຄະນິດສາດທີ່ຕ້ອງການ.ຫານມວນຂອງອົງປະກອບດ້ວຍມວນທັງofົດຂອງທາດປະສົມແລະຄູນດ້ວຍ 100. ຜົນໄດ້ຮັບແມ່ນເປີເຊັນມະຫາຊົນຂອງທາດ. - ຕົວຢ່າງ 1: ເປີເຊັນຂອງມະຫາຊົນ = (ມວນໂມເລກຸນຂອງອົງປະກອບ / ມວນສານໂມເລກຸນທັງofົດຂອງທາດປະສົມ) x 100 = (2.01588 / 18.01528) x 100 = 0.111189 x 100 = 11.18%. ດັ່ງນັ້ນ, ອັດຕາສ່ວນມວນສານຂອງປະລໍາມະນູໄຮໂດເຈນໃນໂມເລກຸນນໍ້າແມ່ນ 11.18%.
- ຕົວຢ່າງ 2: ເປີເຊັນຂອງມະຫາຊົນ = (ມວນໂມເລກຸນຂອງອົງປະກອບ / ມວນສານໂມເລກຸນທັງofົດຂອງສານປະສົມ) x 100 = (72.0642 / 180.156) x 100 = 0.4000 x 100 = 40.00%. ດັ່ງນັ້ນ, ອັດຕາສ່ວນນໍ້າ ໜັກ ຂອງອະຕອມຄາບອນໃນໂມເລກຸນນໍ້າຕານແມ່ນ 40.00%.