ກະວີ:
Helen Garcia
ວັນທີຂອງການສ້າງ:
21 ເດືອນເມສາ 2021
ວັນທີປັບປຸງ:
1 ເດືອນກໍລະກົດ 2024
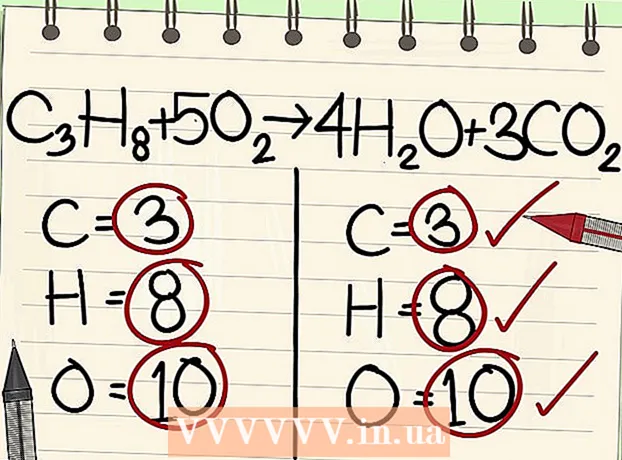
ເນື້ອຫາ
ສົມຜົນທາງເຄມີແມ່ນເປັນຕົວແທນຂອງປະຕິກິລິຍາທາງເຄມີ. ໃນກໍລະນີນີ້, ທາດປະສົມທີ່ມີປະຕິກິລິຍາຖືກຂຽນຢູ່ເບື້ອງຊ້າຍ, ແລະສານທີ່ໄດ້ຜົນ (ຜະລິດຕະພັນປະຕິກິລິຍາ) - ຢູ່ເບື້ອງຂວາຂອງສົມຜົນ. ລູກສອນຖືກວາງຢູ່ລະຫວ່າງພວກມັນຈາກຊ້າຍຫາຂວາ, ເຊິ່ງສະແດງເຖິງທິດທາງຂອງປະຕິກິລິຍາ. ອີງຕາມກົດofາຍຂອງການອະນຸລັກມວນສານ, ໃນໄລຍະທີ່ມີປະຕິກິລິຍາທາງເຄມີ, ອະຕອມໃcannot່ບໍ່ສາມາດປະກົດຂຶ້ນໄດ້ຫຼືຂອງເກົ່າຫາຍໄປ; . ບົດຄວາມນີ້ອະທິບາຍວິທີການດຸ່ນດ່ຽງສົມຜົນທາງເຄມີໂດຍໃຊ້ວິທີການຕ່າງ different.
ຂັ້ນຕອນ
ວິທີທີ 1 ໃນ 2: ວິທີດັ້ງເດີມ
 1 ຂຽນສົມຜົນທາງເຄມີ. ເປັນຕົວຢ່າງ, ພິຈາລະນາປະຕິກິລິຍາຕໍ່ໄປນີ້:
1 ຂຽນສົມຜົນທາງເຄມີ. ເປັນຕົວຢ່າງ, ພິຈາລະນາປະຕິກິລິຍາຕໍ່ໄປນີ້: - ຄ3ຮ8 + ໂອ2 -> ຮ2O + CO2
- ປະຕິກິລິຍານີ້ອະທິບາຍເຖິງການເຜົາໄof້ຂອງ propane (C.3ຮ8) ຢູ່ໃນສະພາບທີ່ມີອົກຊີເຈນເພື່ອປະກອບເປັນນໍ້າແລະຄາບອນໄດອອກໄຊ (ຄາບອນໄດອອກໄຊ).
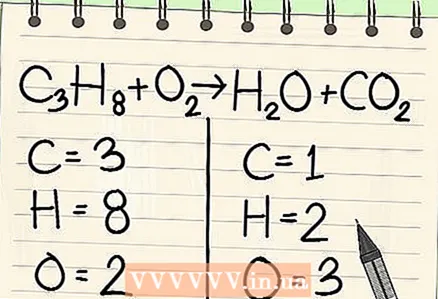 2 ຂຽນຈໍານວນປະລໍາມະນູສໍາລັບແຕ່ລະອົງປະກອບ. ເຮັດອັນນີ້ສໍາລັບທັງສອງດ້ານຂອງສົມຜົນ. ໃຫ້ສັງເກດຕົວຫຍໍ້ທີ່ຢູ່ຖັດຈາກແຕ່ລະອົງປະກອບເພື່ອກໍານົດຈໍານວນອະຕອມທັງົດ. ຂຽນສັນຍາລັກສໍາລັບແຕ່ລະອົງປະກອບໃນສົມຜົນແລະບັນທຶກຈໍານວນອະຕອມທີ່ສອດຄ້ອງກັນ.
2 ຂຽນຈໍານວນປະລໍາມະນູສໍາລັບແຕ່ລະອົງປະກອບ. ເຮັດອັນນີ້ສໍາລັບທັງສອງດ້ານຂອງສົມຜົນ. ໃຫ້ສັງເກດຕົວຫຍໍ້ທີ່ຢູ່ຖັດຈາກແຕ່ລະອົງປະກອບເພື່ອກໍານົດຈໍານວນອະຕອມທັງົດ. ຂຽນສັນຍາລັກສໍາລັບແຕ່ລະອົງປະກອບໃນສົມຜົນແລະບັນທຶກຈໍານວນອະຕອມທີ່ສອດຄ້ອງກັນ. - ຕົວຢ່າງ, ຢູ່ເບື້ອງຂວາຂອງສົມຜົນທີ່ຢູ່ພາຍໃຕ້ການພິຈາລະນາ, ຜົນຂອງການເພີ່ມເຕີມ, ພວກເຮົາໄດ້ຮັບ 3 ປະລໍາມະນູອົກຊີ.
- ຢູ່ເບື້ອງຊ້າຍ, ພວກເຮົາມີອະຕອມຄາບອນ 3 ໜ່ວຍ (C.3), 8 ປະລໍາມະນູໄຮໂດຣເຈນ (H8) ແລະ 2 ປະລໍາມະນູອົກຊີ (O2).
- ຢູ່ເບື້ອງຂວາພວກເຮົາມີ 1 ປະລໍາມະນູກາກບອນ (C), 2 ປະລໍາມະນູໄຮໂດຣເຈນ (H.2) ແລະ 3 ປະລໍາມະນູອົກຊີ (O + O2).
 3 ບັນທຶກໄຮໂດເຈນແລະອົກຊີໄວ້ໃນພາຍຫຼັງ, ເພາະວ່າມັນເປັນສ່ວນ ໜຶ່ງ ຂອງທາດປະສົມຫຼາຍອັນຢູ່ທາງເບື້ອງຊ້າຍແລະຂວາ. ໄຮໂດເຈນແລະອົກຊີແມ່ນສ່ວນ ໜຶ່ງ ຂອງໂມເລກຸນຫຼາຍ ໜ່ວຍ, ສະນັ້ນມັນດີທີ່ສຸດທີ່ຈະເຮັດໃຫ້ມັນສົມດຸນກັນ.
3 ບັນທຶກໄຮໂດເຈນແລະອົກຊີໄວ້ໃນພາຍຫຼັງ, ເພາະວ່າມັນເປັນສ່ວນ ໜຶ່ງ ຂອງທາດປະສົມຫຼາຍອັນຢູ່ທາງເບື້ອງຊ້າຍແລະຂວາ. ໄຮໂດເຈນແລະອົກຊີແມ່ນສ່ວນ ໜຶ່ງ ຂອງໂມເລກຸນຫຼາຍ ໜ່ວຍ, ສະນັ້ນມັນດີທີ່ສຸດທີ່ຈະເຮັດໃຫ້ມັນສົມດຸນກັນ. - ກ່ອນການດຸ່ນດ່ຽງໄຮໂດເຈນແລະອົກຊີເຈນ, ເຈົ້າຈະຕ້ອງໄດ້ຄິດໄລ່ປະລໍາມະນູອີກເທື່ອ ໜຶ່ງ, ເນື່ອງຈາກປັດໃຈເພີ່ມເຕີມອາດຈະຈໍາເປັນເພື່ອດຸ່ນດ່ຽງອົງປະກອບອື່ນ other.
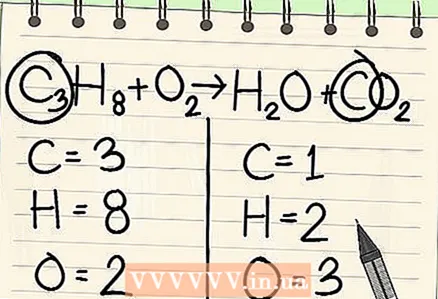 4 ເລີ່ມຕົ້ນດ້ວຍລາຍການທີ່ມີ ໜ້ອຍ ທີ່ສຸດ. ຖ້າເຈົ້າຕ້ອງການດຸ່ນດ່ຽງອົງປະກອບຫຼາຍອັນ, ເລືອກອັນທີ່ເປັນສ່ວນ ໜຶ່ງ ຂອງໂມເລກຸນນໍ້າຢາຊະນິດ ໜຶ່ງ ແລະຜະລິດຕະພັນປະຕິກິລິຍາ ໜຶ່ງ ໂມເລກຸນ. ສະນັ້ນ, ກາກບອນຕ້ອງດຸ່ນດ່ຽງກ່ອນ.
4 ເລີ່ມຕົ້ນດ້ວຍລາຍການທີ່ມີ ໜ້ອຍ ທີ່ສຸດ. ຖ້າເຈົ້າຕ້ອງການດຸ່ນດ່ຽງອົງປະກອບຫຼາຍອັນ, ເລືອກອັນທີ່ເປັນສ່ວນ ໜຶ່ງ ຂອງໂມເລກຸນນໍ້າຢາຊະນິດ ໜຶ່ງ ແລະຜະລິດຕະພັນປະຕິກິລິຍາ ໜຶ່ງ ໂມເລກຸນ. ສະນັ້ນ, ກາກບອນຕ້ອງດຸ່ນດ່ຽງກ່ອນ. 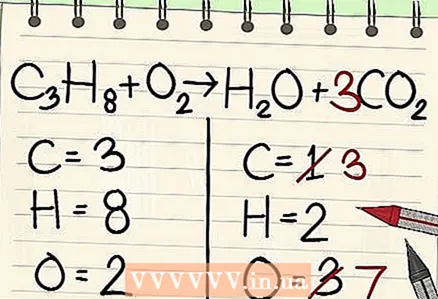 5 ເພື່ອຄວາມສົມດຸນ, ເພີ່ມປັດໃຈຢູ່ທາງ ໜ້າ ຂອງອະຕອມຄາບອນດຽວ. ວາງປັດໃຈຢູ່ທາງ ໜ້າ ຂອງກາກບອນດ່ຽວຢູ່ດ້ານຂວາຂອງສົມຜົນເພື່ອດຸ່ນດ່ຽງມັນດ້ວຍຄາບອນ 3 ຢູ່ເບື້ອງຊ້າຍ.
5 ເພື່ອຄວາມສົມດຸນ, ເພີ່ມປັດໃຈຢູ່ທາງ ໜ້າ ຂອງອະຕອມຄາບອນດຽວ. ວາງປັດໃຈຢູ່ທາງ ໜ້າ ຂອງກາກບອນດ່ຽວຢູ່ດ້ານຂວາຂອງສົມຜົນເພື່ອດຸ່ນດ່ຽງມັນດ້ວຍຄາບອນ 3 ຢູ່ເບື້ອງຊ້າຍ. - ຄ3ຮ8 + ໂອ2 -> ຮ2O + 3CO2
- ປັດໃຈຂອງ 3 ຢູ່ທາງ ໜ້າ ຂອງຄາບອນຢູ່ເບື້ອງຂວາຂອງສົມຜົນຊີ້ໃຫ້ເຫັນວ່າມີສາມປະລໍາມະນູກາກບອນ, ເຊິ່ງກົງກັບສາມປະລໍາມະນູກາກບອນຢູ່ໃນໂມເລກຸນ propane ຢູ່ເບື້ອງຊ້າຍ.
- ໃນສົມຜົນທາງເຄມີ, ເຈົ້າສາມາດປ່ຽນຕົວຄູນຢູ່ທາງ ໜ້າ ຂອງອະຕອມແລະໂມເລກຸນ, ແຕ່ຕົວຫຍໍ້ຈະຕ້ອງບໍ່ປ່ຽນແປງ.
 6 ຈາກນັ້ນດຸ່ນດ່ຽງປະລໍາມະນູ hydrogen. ຫຼັງຈາກທີ່ເຈົ້າໄດ້ເຮັດໃຫ້ຈໍານວນຂອງປະລໍາມະນູກາກບອນຢູ່ດ້ານຊ້າຍແລະຂວາເທົ່າກັນ, ໄຮໂດເຈນແລະອົກຊີເຈນຍັງບໍ່ດຸ່ນດ່ຽງ. ເບື້ອງຊ້າຍຂອງສົມຜົນມີ 8 ອະຕອມໄຮໂດເຈນ, ຕົວເລກດຽວກັນຄວນຢູ່ທາງຂວາ. ບັນລຸເປົ້າthisາຍນີ້ດ້ວຍອັດຕາສ່ວນ.
6 ຈາກນັ້ນດຸ່ນດ່ຽງປະລໍາມະນູ hydrogen. ຫຼັງຈາກທີ່ເຈົ້າໄດ້ເຮັດໃຫ້ຈໍານວນຂອງປະລໍາມະນູກາກບອນຢູ່ດ້ານຊ້າຍແລະຂວາເທົ່າກັນ, ໄຮໂດເຈນແລະອົກຊີເຈນຍັງບໍ່ດຸ່ນດ່ຽງ. ເບື້ອງຊ້າຍຂອງສົມຜົນມີ 8 ອະຕອມໄຮໂດເຈນ, ຕົວເລກດຽວກັນຄວນຢູ່ທາງຂວາ. ບັນລຸເປົ້າthisາຍນີ້ດ້ວຍອັດຕາສ່ວນ. - ຄ3ຮ8 + ໂອ2 -> 4 ຮ2O + 3CO2
- ພວກເຮົາໄດ້ເພີ່ມປັດໄຈ 4 ໃສ່ທາງຂວາ, ເນື່ອງຈາກວ່າຕົວຫຍໍ້ສະແດງໃຫ້ເຫັນວ່າພວກເຮົາມີອະຕອມໄຮໂດເຈນສອງອັນຢູ່ແລ້ວ.
- ຖ້າເຈົ້າຄູນປັດໄຈ 4 ດ້ວຍຕົວຫ້ອຍ 2, ເຈົ້າຈະໄດ້ 8.
- ດ້ວຍເຫດນັ້ນ, ໄດ້ຮັບປະລໍາມະນູອົກຊີແຊນ 10 ອັນຢູ່ທາງເບື້ອງຂວາ: 3x2 = 6 ປະລໍາມະນູໃນສາມໂມເລກຸນ 3CO2 ແລະອີກສີ່ອະຕອມໃນສີ່ໂມເລກຸນຂອງນໍ້າ.
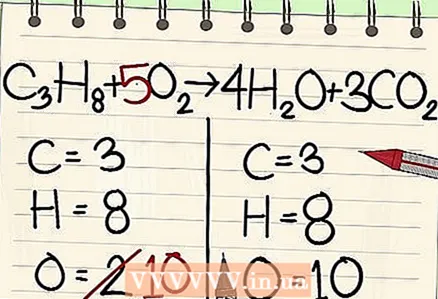 7 ດຸ່ນດ່ຽງປະລໍາມະນູອົກຊີເຈນ. ຈື່ໄວ້ວ່າຕ້ອງປັດໃຈຕົວຄູນທີ່ເຈົ້າໃຊ້ເພື່ອດຸ່ນດ່ຽງອະຕອມອື່ນ other. ເນື່ອງຈາກວ່າເຈົ້າໄດ້ເພີ່ມຕົວຄູນຢູ່ທາງ ໜ້າ ຂອງໂມເລກຸນຢູ່ເບື້ອງຂວາຂອງສົມຜົນ, ຈຳ ນວນຂອງປະລໍາມະນູອົກຊີໄດ້ປ່ຽນໄປ. ດຽວນີ້ເຈົ້າມີ 4 ປະລໍາມະນູອົກຊີໃນໂມເລກຸນນໍ້າແລະ 6 ປະລໍາມະນູອົກຊີໃນໂມເລກຸນຄາບອນໄດອອກໄຊ. ດັ່ງນັ້ນ, ມີ 10 ປະລໍາມະນູອົກຊີໃນດ້ານຂວາ.
7 ດຸ່ນດ່ຽງປະລໍາມະນູອົກຊີເຈນ. ຈື່ໄວ້ວ່າຕ້ອງປັດໃຈຕົວຄູນທີ່ເຈົ້າໃຊ້ເພື່ອດຸ່ນດ່ຽງອະຕອມອື່ນ other. ເນື່ອງຈາກວ່າເຈົ້າໄດ້ເພີ່ມຕົວຄູນຢູ່ທາງ ໜ້າ ຂອງໂມເລກຸນຢູ່ເບື້ອງຂວາຂອງສົມຜົນ, ຈຳ ນວນຂອງປະລໍາມະນູອົກຊີໄດ້ປ່ຽນໄປ. ດຽວນີ້ເຈົ້າມີ 4 ປະລໍາມະນູອົກຊີໃນໂມເລກຸນນໍ້າແລະ 6 ປະລໍາມະນູອົກຊີໃນໂມເລກຸນຄາບອນໄດອອກໄຊ. ດັ່ງນັ້ນ, ມີ 10 ປະລໍາມະນູອົກຊີໃນດ້ານຂວາ. - ເພີ່ມປັດໄຈ 5 ໃຫ້ກັບໂມເລກຸນອົກຊີຢູ່ທາງເບື້ອງຊ້າຍຂອງສົມຜົນ. ດຽວນີ້ແຕ່ລະຊິ້ນສ່ວນປະກອບດ້ວຍ 10 ປະລໍາມະນູອົກຊີເຈນ.
- ຄ3ຮ8 + 5O2 -> 4 ຮ2O + 3CO2.

- ດັ່ງນັ້ນ, ທັງສອງດ້ານຂອງສົມຜົນບັນຈຸມີຈໍານວນຄາບອນ, ໄຮໂດຣເຈນ, ແລະປະລໍາມະນູອົກຊີ. ສົມຜົນແມ່ນສົມດຸນ.
ວິທີທີ 2 ຂອງ 2: ວິທີພຶດຊະຄະນິດ
- 1 ຂຽນສົມຜົນປະຕິກິລິຍາລົງ. ເປັນຕົວຢ່າງ, ພິຈາລະນາປະຕິກິລິຍາທາງເຄມີຕໍ່ໄປນີ້:
- PCl5 + ຮ2O -> ຮ3ຕູ້ໄປສະນີ4 + HCl
- 2 ໃສ່ຈົດinາຍຢູ່ທາງ ໜ້າ ຂອງການເຊື່ອມຕໍ່ແຕ່ລະອັນ:
- ກPCl5 + ຂຮ2ໂອ -> ຄຮ3ຕູ້ໄປສະນີ4 + ງHCl
- 3 ເຮັດໃຫ້ຈໍານວນຂອງປະລໍາມະນູເທົ່າທຽມກັນສໍາລັບແຕ່ລະອົງປະກອບຢູ່ເບື້ອງຊ້າຍແລະຂວາຂອງສົມຜົນ.
- ກPCl5 + ຂຮ2ໂອ -> ຄຮ3ຕູ້ໄປສະນີ4 + ງHCl
- ຢູ່ເບື້ອງຊ້າຍພວກເຮົາມີ 2ຂ ປະລໍາມະນູໄຮໂດເຈນ (2 ໃນແຕ່ລະ H.2O), ໃນຂະນະທີ່ຢູ່ເບື້ອງຂວາແມ່ນ 3ຄ+ງ ປະລໍາມະນູໄຮໂດເຈນ (3 ໃນແຕ່ລະຮ3ຕູ້ໄປສະນີ4 ແລະ 1 ໃນແຕ່ລະໂມເລກຸນ HCl). ເນື່ອງຈາກທັງສອງດ້ານຊ້າຍແລະຂວາຕ້ອງປະກອບດ້ວຍຈໍານວນຂອງປະລໍາມະນູໄຮໂດເຈນ, 2ຂ ຄວນຈະເທົ່າກັບ 3ຄ+ງ.
- ເຮັດສິ່ງນີ້ສໍາລັບອົງປະກອບທັງຫມົດ:
- P: ກ=ຄ
- Cl: 5ກ=ງ
- H: 2ຂ=3ຄ+ງ
- 4 ແກ້ໄຂລະບົບສົມຜົນເພື່ອຊອກຫາຄ່າຕົວເລກຂອງຕົວຄູນ. ລະບົບມີຫຼາຍວິທີແກ້ໄຂ, ເພາະວ່າມີຕົວແປຫຼາຍກວ່າສົມຜົນ. ມັນເປັນສິ່ງ ຈຳ ເປັນທີ່ຈະຕ້ອງຫາວິທີແກ້ໄຂບັນຫາດັ່ງນັ້ນຕົວຄູນທັງhaveົດມີຮູບແບບຂອງ ຈຳ ນວນເຕັມນ້ອຍທີ່ສຸດເທົ່າທີ່ເປັນໄປໄດ້.
- ເພື່ອແກ້ໄຂລະບົບສົມຜົນຢ່າງໄວ, ກຳ ນົດຄ່າຕົວເລກໃຫ້ ໜຶ່ງ ໃນຕົວແປ. ສົມມຸດວ່າ a = 1. ໃຫ້ແກ້ໄຂລະບົບແລະຊອກຫາຄ່າຂອງຕົວແປທີ່ຍັງເຫຼືອ:
- ສຳ ລັບ P a = c, ສະນັ້ນ c = 1
- ສໍາລັບ Cl 5a = d, ເພາະສະນັ້ນ d = 5
- ເນື່ອງຈາກສໍາລັບ H 2b = 3c + d, ພວກເຮົາຊອກຫາຄ່າ b:
- 2b = 3 (1) + 5
- 2b = 3 + 5
- 2b = 8
- b = 4
- ດັ່ງນັ້ນ, ພວກເຮົາມີຕົວຄູນຕໍ່ໄປນີ້:
- a = 1
- b = 4
- c = 1
- d = 5
ຄໍາແນະນໍາ
- ຖ້າເຈົ້າປະສົບກັບຄວາມຫຍຸ້ງຍາກ, ເຄື່ອງຄິດເລກອອນໄລນ can ສາມາດຖືກນໍາໃຊ້ເພື່ອດຸ່ນດ່ຽງສົມຜົນທາງເຄມີ. ແນວໃດກໍ່ຕາມ, ກະລຸນາຮັບຊາບວ່າເຄື່ອງຄິດເລກດັ່ງກ່າວບໍ່ໄດ້ຮັບອະນຸຍາດໃຫ້ໃຊ້ໃນລະຫວ່າງການສອບເສັງ, ສະນັ້ນຢ່າອີງໃສ່ມັນພຽງຢ່າງດຽວ.
- ຈືຂໍ້ມູນການ, ບາງຄັ້ງສົມຜົນສາມາດເຮັດໄດ້ງ່າຍ! ຖ້າຫາກວ່າຄ່າ ສຳ ປະສິດທັງareົດແມ່ນສາມາດຫານດ້ວຍ ຈຳ ນວນເຕັມໄດ້, ໃຫ້ສົມຜົນງ່າຍຂຶ້ນ.
ຄຳ ເຕືອນ
- ເພື່ອກໍາຈັດຄ່າສໍາປະສິດຂອງເສດສ່ວນ, ໃຫ້ຄູນສົມຜົນທັງ(ົດ (ທັງສອງເບື້ອງຊ້າຍແລະຂວາຂອງມັນ) ໂດຍຕົວຫານຂອງເສດສ່ວນ.
- ຢ່າໃຊ້ເສດສ່ວນເປັນຕົວຄູນຂອງສົມຜົນເຄມີ - ບໍ່ມີໂມເລກຸນຫຼືປະລໍາມະນູເຄິ່ງໃນປະຕິກິລິຍາທາງເຄມີ.
- ໃນຂະບວນການດຸ່ນດ່ຽງ, ເຈົ້າສາມາດໃຊ້ເສດສ່ວນເພື່ອຄວາມສະດວກສະບາຍ, ແຕ່ສົມຜົນບໍ່ສົມດຸນຕາບໃດທີ່ຍັງມີຕົວຄູນປະກອບສ່ວນຢູ່ໃນນັ້ນ.



