ກະວີ:
Monica Porter
ວັນທີຂອງການສ້າງ:
17 ດົນໆ 2021
ວັນທີປັບປຸງ:
1 ເດືອນກໍລະກົດ 2024

ເນື້ອຫາ
ຄວາມເຂັ້ມຂົ້ນຂອງ Molar ສະແດງໃຫ້ເຫັນຄວາມ ສຳ ພັນລະຫວ່າງ ຈຳ ນວນໂມເລກຸນຂອງລະລາຍແລະປະລິມານການແກ້ໄຂ. ເພື່ອຄິດໄລ່ຄວາມຊື້ນ, ທ່ານສາມາດເລີ່ມຕົ້ນດ້ວຍ moles ແລະປະລິມານ, ມວນແລະບໍລິມາດ, ຫຼື moles ແລະ millilit ລິດ (ml). ຈາກນັ້ນ, ດ້ວຍຕົວແປຕ່າງໆທີ່ຢູ່ຂ້າງເທິງ, ນຳ ໃຊ້ສູດສູດຄວາມເຂັ້ມຂົ້ນຂັ້ນພື້ນຖານເພື່ອໃຫ້ໄດ້ຜົນທີ່ຖືກຕ້ອງ.
ຂັ້ນຕອນ
ວິທີທີ່ 1 ຂອງ 4: ຄິດໄລ່ຄວາມເຂັ້ມຂົ້ນຂອງ Mol ຈາກ ຈຳ ນວນ Molar ແລະ ຈຳ ນວນ
ມັນເປັນສິ່ງສໍາຄັນທີ່ຈະຮູ້ສູດພື້ນຖານ ສຳ ລັບການຄິດໄລ່ຄວາມເຂັ້ມຂົ້ນຂອງໂມໂມ. ຄວາມເຂັ້ມຂົ້ນຂອງ Molar ເທົ່າກັບ ຈຳ ນວນ moles ຂອງ solute ແບ່ງອອກໂດຍປະລິມານຂອງໂຊລູຊັ່ນໃນລິດ. ຈາກນັ້ນ, ພວກເຮົາມີສູດດັ່ງຕໍ່ໄປນີ້: ຄວາມເຂັ້ມຂຸ້ນຂອງ Molar = ຈຳ ນວນ moles ຂອງການລະລາຍ / ຈຳ ນວນລິດຂອງລິດ
- ຕົວຢ່າງ: ຄວາມເຂັ້ມຂຸ້ນຂອງໂມເລກຸນຂອງໂຊລູຊັ່ນບັນຈຸ 0,75 mol NaCl ໃນ 4.2 ລິດແມ່ນແນວໃດ?

ວິເຄາະຫົວຂໍ້. ເພື່ອຄິດໄລ່ຄວາມເຂັ້ມຂົ້ນຂອງໂມໂມ, ທ່ານຕ້ອງການ ຈຳ ນວນຂອງ moles ແລະປະລິມານການແກ້ໄຂໃນລິດ. ທ່ານບໍ່ ຈຳ ເປັນຕ້ອງຄິດໄລ່ຄ່າສອງຢ່າງນີ້ເພາະຫົວຂໍ້ທີ່ທ່ານໃຫ້.- ຍົກຕົວຢ່າງ:
- ຈໍານວນຂອງ moles = 0.75 moles ຂອງ NaCl
- ປະລິມານ = 4.2 ລິດ
- ຍົກຕົວຢ່າງ:
ແບ່ງ ຈຳ ນວນຂອງ moles ຕາມປະລິມານ. ຜົນຂອງການແບ່ງລະດັບໂມເລກຸນຕາມປະລິມານແມ່ນ ຈຳ ນວນໂມເລກຸນຕໍ່ລິດ, ຫຼືຄວາມເຂັ້ມຂຸ້ນຂອງໂມເລກຸນຂອງວິທີແກ້ໄຂນັ້ນ.
- ຕົວຢ່າງ: ຄວາມເຂັ້ມຂຸ້ນຂອງ molar = ຈຳ ນວນໂມເລກຸນລະລາຍ / ຈຳ ນວນລິດຂອງລິດ = 0.75 mol / 4.2 L = 0.17857142

ບັນທຶກຜົນໄດ້ຮັບຂອງທ່ານ. ຮອບສອງຫາສາມຕົວເລກຫຼັງຈາກທີ່ເຄື່ອງ ໝາຍ, ຂື້ນກັບ ຄຳ ຮ້ອງຂໍຂອງຄູຫຼືການມອບ ໝາຍ. ເມື່ອບັນທຶກຜົນໄດ້ຮັບຂອງທ່ານ, ຫຍໍ້ "ຄວາມເຂັ້ມຂຸ້ນຂອງໂມ້" ກັບ "M" ແລະລວມເອົາສັນຍາລັກເຄມີຂອງສານລະລາຍ.- ຍົກຕົວຢ່າງ: 0.179 M NaCl
ວິທີທີ່ 2 ຂອງ 4: ຄິດໄລ່ຄວາມເຂັ້ມຂົ້ນຂອງໂມນຈາກມະຫາຊົນແລະບໍລິມາດ
ມັນເປັນສິ່ງຈໍາເປັນທີ່ຈະຕ້ອງຮູ້ສູດພື້ນຖານສໍາລັບການຄິດໄລ່ຄວາມເຂັ້ມຂົ້ນຂອງໂມໂມ. ຄວາມເຂັ້ມຂົ້ນຂອງ Molar ສະແດງໃຫ້ເຫັນຄວາມ ສຳ ພັນລະຫວ່າງ ຈຳ ນວນໂມເລກຸນຂອງລະລາຍແລະປະລິມານການແກ້ໄຂ. ສູດ ສຳ ລັບຄວາມເຂັ້ມຂົ້ນຂອງໂມຣາແມ່ນມີດັ່ງນີ້: ຄວາມເຂັ້ມຂຸ້ນຂອງ molar = ຄວາມເຂັ້ມຂຸ້ນຂອງ solute / ຈຳ ນວນລິດຂອງໂຊລູຊັ່ນ
- ຕົວຢ່າງຂອງປັນຫາ: ຄິດໄລ່ ຈຳ ນວນຂອງວິທີແກ້ໄຂເມື່ອລະລາຍ 3,4 g ຂອງ KMnO4 ໃນນ້ ຳ 5,2 ລິດ.

ວິເຄາະຫົວຂໍ້: ເພື່ອຊອກຫາຄວາມເຂັ້ມຂົ້ນຂອງ molar, ທ່ານຕ້ອງການ ຈຳ ນວນຂອງ moles ແລະປະລິມານການແກ້ໄຂໃນລິດ. ຖ້າຄຸນຄ່າເຫລົ່ານີ້ບໍ່ໄດ້ຖືກມອບໃຫ້, ແຕ່ທ່ານຮູ້ປະລິມານແລະມວນສານຂອງວິທີແກ້ໄຂ, ທ່ານສາມາດ ກຳ ນົດ ຈຳ ນວນຂອງການລະລາຍກ່ອນທີ່ຈະຄິດໄລ່ຄວາມເຂັ້ມຂົ້ນຂອງໂມໂມ.- ຍົກຕົວຢ່າງ:
- ນໍ້າ ໜັກ = 3.4 g KMnO4
- ປະລິມານ = 5.2 ລ
- ຍົກຕົວຢ່າງ:
ຄິດໄລ່ໂມເລກຸນມວນສານຂອງລະລາຍ. ເພື່ອຄິດໄລ່ ຈຳ ນວນໂມເລກຸນຂອງເຈືອຈາງຈາກມະຫາຊົນນັ້ນຫຼືກຼາມຂອງການລະລາຍ, ທຳ ອິດທ່ານຕ້ອງ ກຳ ນົດໂມເລກຸນຂອງ solute. ໂມເລກຸນມວນຂອງລະລາຍສາມາດ ກຳ ນົດໄດ້ໂດຍການເພີ່ມປະລິມານມະຫາຊົນຂອງແຕ່ລະອົງປະກອບໃນການແກ້ໄຂ. ເພື່ອຊອກຫາປະລໍາມະນູກ້ອນຂອງແຕ່ລະອົງປະກອບ, ໃຫ້ໃຊ້ຕາຕະລາງແຕ່ລະໄລຍະຂອງອົງປະກອບ.
- ຍົກຕົວຢ່າງ:
- ປະລິມານມະຫາຊົນຂອງ K = 39.1 g
- ປະລິມານມະຫາຊົນຂອງ Mn = 54.9 g
- ປະລິມານມະຫາຊົນຂອງ O = 16,0 g
- ປະລິມານທັງ ໝົດ ຂອງມວນ = K + Mn + O + O + O = O = 39.1 + 54.9 + 16 + 16 + 16 + 16 = 158.0 ກ
- ຍົກຕົວຢ່າງ:
ປ່ຽນກຼາມເປັນ moles. ເມື່ອທ່ານມີໂມເລກຸນກ້ອນ ໜຶ່ງ, ທ່ານ ຈຳ ເປັນຕ້ອງຄູນ ຈຳ ນວນກຼາມຂອງທາດລະລາຍໃນວິທີແກ້ໄຂໂດຍປັດໃຈການປ່ຽນຂອງ 1 ມລຕໍ່ກ້ອນມະຫາຊົນຂອງສານລະລາຍ. ຜົນຂອງການຄູນນີ້ແມ່ນ ຈຳ ນວນຂອງໂຕລະລາຍ.
- ຕົວຢ່າງ: ກຼາມຂອງທາດລະລາຍ * (1 / ມະຫາຊົນຂອງທາດລະລາຍ) = 3.4 g * (1 mol / 158 g) = 0.0215 mol
ແບ່ງ ຈຳ ນວນໂມ້ຕາມ ຈຳ ນວນລິດ. ດຽວນີ້ທ່ານໄດ້ຄິດໄລ່ ຈຳ ນວນຂອງ moles, ຕອນນີ້ແບ່ງ ຈຳ ນວນນັ້ນໂດຍປະລິມານຂອງວິທີແກ້ໄຂໃນລິດ, ທ່ານຈະມີຄວາມເຂັ້ມຂຸ້ນຂອງໂມເລກຸນຂອງວິທີແກ້ໄຂນັ້ນ.
- ຕົວຢ່າງ: ຄວາມເຂັ້ມຂຸ້ນຂອງ molar = ຈຳ ນວນໂມເລກຸນລະລາຍ / ຈຳ ນວນລິດຂອງລິດ = 0.0215 mol / 5.2 L = 0.004134615
ບັນທຶກຜົນໄດ້ຮັບຂອງທ່ານ. ທ່ານ ຈຳ ເປັນຕ້ອງລວບລວມຜົນໄດ້ຮັບຕາມຄວາມຕ້ອງການຂອງອາຈານ, ໂດຍປົກກະຕິແມ່ນສອງຫາສາມຕົວເລກຫຼັງຈາກທີ່ມີເຄື່ອງ ໝາຍ ຈຸດ. ນອກຈາກນັ້ນ, ໃນເວລາທີ່ຂຽນຜົນໄດ້ຮັບ, ໃຫ້ຫຍໍ້ "ຄວາມເຂັ້ມຂຸ້ນຂອງ molar" ເປັນ "M" ແລະພ້ອມກັບສັນຍາລັກເຄມີຂອງສານລະລາຍ.
- ຍົກຕົວຢ່າງ: 0.004 M KMnO4
ວິທີທີ 3 ຂອງ 4: ຄິດໄລ່ຄວາມເຂັ້ມຂົ້ນຂອງ Molar ຈາກ ຈຳ ນວນຂອງ moles ແລະ Millilitic solution
ຈຳ ເປັນຕ້ອງຮູ້ສູດ ສຳ ລັບຄວາມເຂັ້ມຂົ້ນຂອງໂມຣາ. ເພື່ອຄິດໄລ່ຄວາມເຂັ້ມຂົ້ນຂອງໂມວ. ທ່ານ ຈຳ ເປັນຕ້ອງຄິດໄລ່ ຈຳ ນວນຂອງນ້ ຳ ມັນລະລາຍຕໍ່ລິດ, ບໍ່ແມ່ນມິນລິລິດຂອງວິທີແກ້ໄຂ. ສູດທົ່ວໄປ ສຳ ລັບການຄິດໄລ່ຄວາມເຂັ້ມຂົ້ນຂອງໂມວແມ່ນ: ຄວາມເຂັ້ມຂຸ້ນຂອງ molar = ຈຳ ນວນ moles ຂອງການລະລາຍ / ຈຳ ນວນລິດຂອງລິດ
- ຕົວຢ່າງ: ຄິດໄລ່ຄວາມເຂັ້ມຂຸ້ນຂອງໂມມູນຂອງວິທີແກ້ໄຂບັນຈຸ 1.2 moles ຂອງ CaCl2 ໃນນ້ ຳ 2905 ມິນລີລິດ.
ວິເຄາະຫົວຂໍ້. ເພື່ອຄິດໄລ່ຄວາມເຂັ້ມຂົ້ນຂອງໂມລາ, ທ່ານ ຈຳ ເປັນຕ້ອງມີ ຈຳ ນວນໂມເລກຸນລະລາຍແລະປະລິມານການແກ້ໄຂເປັນລິດ ຖ້າປະລິມານການແກ້ໄຂບັນຫາມີໃນບັນຫາໃນມິນລິລິດ, ໃຫ້ປ່ຽນເປັນປະລິມານທຽບເທົ່າເປັນລິດກ່ອນທີ່ຈະຄິດໄລ່.
- ຍົກຕົວຢ່າງ:
- ຈໍານວນຂອງ moles = 1.2 moles ຂອງ CaCl2
- ປະລິມານ = 2905 ml
- ຍົກຕົວຢ່າງ:
ແປງມິນລີລິດເປັນລິດ. ເພື່ອປ່ຽນວິທີແກ້ໄຂຈາກມິນລີລິດເປັນລິດ, ແບ່ງ ຈຳ ນວນມິນລີລິດໃຫ້ເປັນ 1000, ເພາະວ່າແຕ່ລະລິດເທົ່າກັບ 1000 ມິນລີລິດ. ທ່ານຍັງສາມາດປ່ຽນເປັນມິນລີລິດເປັນລິດໂດຍປ່ຽນຈຸດທົດສະນິຍົມ 3 ຕົວເລກໄວ້.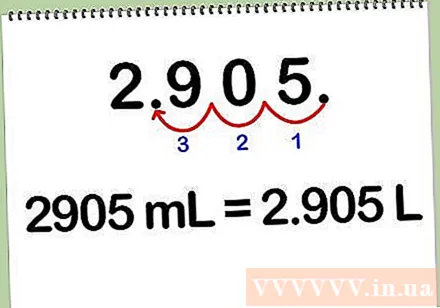
- ຕົວຢ່າງ: 2905 ml * (1 ລິດ / 1000 ມລ) = 2,905 ລ
ແບ່ງ ຈຳ ນວນໂມ້ຕາມ ຈຳ ນວນລິດ. ຫຼັງຈາກທີ່ທ່ານມີ ຈຳ ນວນລິດແລ້ວ, ທ່ານສາມາດຄິດໄລ່ຄວາມເຂັ້ມຂົ້ນຂອງ molar ໂດຍແບ່ງປັນ ຈຳ ນວນຂອງ moles ຕາມ ຈຳ ນວນລິດຂອງລິດ.
- ຕົວຢ່າງ: ຄວາມເຂັ້ມຂຸ້ນຂອງ molar = ຈຳ ນວນ moles ຂອງ solute / ຈຳ ນວນລິດຂອງການແກ້ໄຂ = 1.2 moles ຂອງ CaCl2 / 2,905 L = 0.413080895
ບັນທຶກຜົນໄດ້ຮັບຂອງທ່ານ. ຈືຂໍ້ມູນການໃຫ້ຮອບຜົນໄດ້ຮັບເປັນສອງຫລືສາມຈຸດ, ຫຼືຕາມການຮ້ອງຂໍຂອງຄູອາຈານຂອງທ່ານ. ເມື່ອບັນທຶກຜົນໄດ້ຮັບ, ໃຫ້ຫຍໍ້ "ຄວາມເຂັ້ມຂຸ້ນຂອງ molar" ເປັນ "M" ແລະຫຼັງຈາກນັ້ນແມ່ນສັນຍາລັກທາງເຄມີ ສຳ ລັບການລະລາຍ.
- ຍົກຕົວຢ່າງ: 0.413 M CaCl2
ວິທີທີ 4 ຂອງ 4: ການປະຕິບັດພິເສດ
ຄິດໄລ່ຄວາມເຂັ້ມຂຸ້ນຂອງໂມມູນຂອງວິທີແກ້ໄຂເມື່ອ 5.2 g NaCl ຈະລະລາຍໃນນ້ ຳ 800 ml. ກຳ ນົດຄ່າທີ່ໃຫ້ໂດຍບັນຫາ: ມະຫາຊົນເປັນກຼາມແລະປະລິມານເປັນມິນລິລິດ.
- ມະຫາຊົນ = 5.2 g NaCl
- ປະລິມານ = 800 ml ນ້ ຳ
ຊອກຫາໂມເລກຸນຂອງ NaCl ໂດຍການເພີ່ມປະລໍາມະນູກ້ອນຂອງອົງປະກອບ Na, ແລະປະລໍາມະນູກ້ອນຂອງ Cl.
- ປະລິມານມະຫາຊົນຂອງ Na = 22.99 g
- ປະລິມານມະຫາຊົນຂອງ Cl = 35.45 g
- ໂມເລກຸນມະຫາຊົນຂອງ NaCl = 22.99 + 35.45 = 58.44 g
ຄູນ ຈຳ ນວນມະຫາສານຂອງການລະລາຍໂດຍປັດໃຈການປ່ຽນເມກ. ໃນຕົວຢ່າງນີ້, ໂມເລກຸນຂອງ NaCl ແມ່ນ 58.44 g, ສະນັ້ນປັດໄຈການປ່ຽນໃຈເຫລື້ອມໃສແມ່ນ“ 1 mol / 58.44 g”.
- ຈໍານວນຂອງໂມຄູນ NaCl = 5.2 g NaCl * (1 ມມ / 58,44 ກຣາມ) = 0.8898 mol = 0.09 mol
ແບ່ງນ້ ຳ 800 ml ໂດຍ 1000, ທ່ານຈະໄດ້ຮັບປະລິມານນ້ ຳ ເປັນລິດ.
- ທ່ານຍັງສາມາດເພີ່ມປະລິມານ 800 ມລໂດຍປັດໄຈການປ່ຽນ 1 ລິດ / 1000 ມລຈາກມິນລີລິດເປັນລິດ.
- ເພື່ອເຮັດໃຫ້ຂະບວນການຄູນສັ້ນລົງຂ້າງເທິງ, ທ່ານສາມາດຖອຍຫຼັງຈຸດທະສະນິຍົມ 3 ຕົວເລກຢູ່ເບື້ອງຊ້າຍ.
- ປະລິມານ = 800 ml * (1 ລິດ / 1000 ມລ) = 800 ມລ / 1000 ມລ = 0,8 ລິດ
ແບ່ງ ຈຳ ນວນ moles ຂອງ solute ໂດຍປະລິມານຂອງໂຊລູຊັ່ນໃນລິດ. ເພື່ອຄິດໄລ່ຄວາມເຂັ້ມຂົ້ນຂອງໂມລາ, ທ່ານ ຈຳ ເປັນຕ້ອງແບ່ງຄວາມຈ່ອຍລົງ 0.09 moles (ໃນກໍລະນີນີ້, NaCl) ໂດຍປະລິມານການແກ້ໄຂໃນລິດ.
- ຄວາມເຂັ້ມຂຸ້ນຂອງ Molar = ຈຳ ນວນນ້ ຳ ມັນລະລາຍ / ຈຳ ນວນລິດຕໍ່ລິດ = 0.09 mol / 0.8 L = 0.1125 mol / L
ບັນທຶກຜົນສຸດທ້າຍ. ປິດຜົນໄດ້ຮັບເປັນສອງຫລືສາມຕົວເລກຫຼັງຈາກເຄື່ອງ ໝາຍ ແລະຫຍໍ້ "ຄວາມເຂັ້ມຂຸ້ນຂອງໂມ" ກັບ "M" ພ້ອມກັບສັນຍາລັກເຄມີທີ່ລະລາຍ.
- ຜົນໄດ້ຮັບ: 0.11 M NaCl