ກະວີ:
Louise Ward
ວັນທີຂອງການສ້າງ:
11 ກຸມພາ 2021
ວັນທີປັບປຸງ:
1 ເດືອນກໍລະກົດ 2024

ເນື້ອຫາ
ຂະ ໜາດ ຂອງປະລໍາມະນູແມ່ນມີຂະ ໜາດ ນ້ອຍດັ່ງນັ້ນມັນຍາກທີ່ຈະວັດແທກຕົວເລກປະລໍາມະນູຂອງທາດປະສົມສານເຄມີໄດ້ຢ່າງຖືກຕ້ອງ. ເພື່ອສາມາດວັດປະລິມານຂອງສານໄດ້ຢ່າງຖືກຕ້ອງ, ນັກວິທະຍາສາດໃຊ້ຫົວ ໜ່ວຍ ໂມເລກຸນເພື່ອເປັນຕົວແທນຂອງ ຈຳ ນວນອະຕອມທີ່ລະບຸໄວ້. ທາດໂມເລກຸນ ໜຶ່ງ ໄດ້ຖືກ ກຳ ນົດເທົ່າກັບ ຈຳ ນວນອະຕອມຄາບອນທີ່ບັນຈຸຢູ່ໃນທາດໄອໂຊໂທນຄາບອນ 12 ກຼາມ, ເຊິ່ງມີປະມານ 6,022 x 10 ອະຕອມ. ມູນຄ່ານີ້ເອີ້ນວ່າເລກ Avogadro, ຫຼື Avogadro ຄົງທີ່. ອັນນີ້ຍັງ ໝາຍ ເຖິງ ຈຳ ນວນປະລໍາມະນູໃນ 1 ໂມເລກຸນຂອງອົງປະກອບໃດ ໜຶ່ງ ແລະ 1 ມະຫາສານຂອງທາດນັ້ນເອີ້ນວ່າມະຫາຊົນໂມໂມຂອງສານນັ້ນ.
ຂັ້ນຕອນ
ວິທີທີ່ 1 ຂອງ 2: ຄິດໄລ່ມວນສານໂມໂມຂອງອົງປະກອບໃດ ໜຶ່ງ
ຄໍານິຍາມຂອງມະຫາຊົນ molar. ມະຫາຊົນຂອງໂມເລກຸນຂອງສານແມ່ນມວນ (ເປັນກຼາມ) ຂອງໂມເລກຸນ ໜຶ່ງ ຂອງສານນັ້ນ. ເພື່ອຄິດໄລ່ມວນສານໂມເລກຸນຂອງອົງປະກອບໃດ ໜຶ່ງ, ຄູນມະຫາປະລໍາມະນູຂອງມັນໂດຍປັດໄຈການປ່ຽນເປັນແກັດຕໍ່ກິໂລກຼາມ
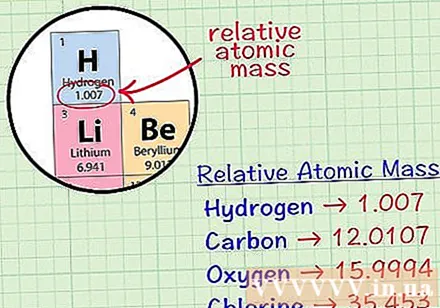
ຊອກຫາປະລໍາມະນູກ້ອນສະເລ່ຍຂອງອົງປະກອບໃດ ໜຶ່ງ. ປະລິມານມະຫາສານສະເລ່ຍຂອງອົງປະກອບໃດ ໜຶ່ງ ແມ່ນມະຫາຊົນສະເລ່ຍ, ໃນຫົວ ໜ່ວຍ ປະລໍາມະນູ, ໃນຕົວຢ່າງ ໜຶ່ງ ເຊິ່ງປະກອບມີ isotopes ທັງ ໝົດ ຂອງອົງປະກອບນັ້ນ. ຂໍ້ມູນນີ້ມັກຈະຖືກມອບໃຫ້ໃນຕາຕະລາງແຕ່ລະໄລຍະຂອງອົງປະກອບ. ໂດຍການຊອກຫາອົງປະກອບໃດ ໜຶ່ງ, ທ່ານສາມາດຊອກຫາປະລໍາມະນູກ້ອນໂດຍສະເລ່ຍທີ່ຂຽນຢູ່ດ້ານລຸ່ມຂອງສັນຍາລັກທາງເຄມີຂອງອົງປະກອບ. ມູນຄ່ານີ້ບໍ່ແມ່ນເລກເຕັມ, ແຕ່ເປັນຕົວເລກທີ່ມີອັດຕານິຍົມ.- ຍົກຕົວຢ່າງ, ດ້ວຍ hydrogen, ປະລິມານມະຫາຊົນສະເລ່ຍແມ່ນ 1.007; ສະເລ່ຍປະລໍາມະນູຂອງຄາບອນແມ່ນ 12,0107; ປະລິມານມະຫາຊົນສະເລ່ຍຂອງອົກຊີເຈນແມ່ນ 15,9994; chlorine ມີມວນສານປະລໍາມະນູສະເລ່ຍ 35,453.

ຄູນປະລິມານມະຫາສະເລ່ຍໂດຍ ຈຳ ນວນມະຫາຊົນຂອງໂມມູນຄົງທີ່. ຫນ່ວຍບໍລິການຂອງເຫລັກຫີນປູນຖືກ ກຳ ນົດເປັນ 0,001 ກິໂລກຼາມຕໍ່ກິໂລກຼາມ, ຫລື 1 ກະລາມຕໍ່ກິໂລກຼາມ. ຜະລິດຕະພັນຂອງອະຕອມມະຫາຊົນສະເລ່ຍແລະມະຫາຊົນໂມເລກຸນຄົງຈະເຮັດໃຫ້ຫນ່ວຍບໍລິສັດມະຫາສະມຸດກາຍເປັນກຼາມຕໍ່ກິໂລກຼາມ, ສະນັ້ນມວນໂມເລກຸນຂອງໂມເລກຸນຈະຢູ່ທີ່ 1,007 ກຼາມຕໍ່ໂມເລກຸນ, ຂອງກາກບອນແມ່ນ 12. , 0107 ກຣາມຕໍ່ໂມເລກຸນ, ຂອງອົກຊີແມ່ນ 15,9995 ກຣາມຕໍ່ໂມເລກຸນ, ແລະທາດ chlorine ແມ່ນ 35,453 ກຼາມຕໍ່ໂມເລກຸນ.- ບາງອົງປະກອບມີຢູ່ໃນ ທຳ ມະຊາດຄືກັບໂມເລກຸນປະກອບດ້ວຍສອງຫຼືຫຼາຍກວ່ານັ້ນຂອງປະລໍາມະນູດຽວກັນ. ນັ້ນແມ່ນ, ຖ້າທ່ານຕ້ອງການທີ່ຈະຄິດໄລ່ມວນສານໂມເລກຸນຂອງທາດປະກອບທີ່ປະກອບດ້ວຍຫຼາຍກວ່າອະຕອມເຊັ່ນ: ອາຍແກັສ hydrogen, ອາຍແກັສອົກຊີເຈນຫຼືອາຍແກັສ chlorine, ທ່ານ ຈຳ ເປັນຕ້ອງ ກຳ ນົດມວນສານປະລະມະນູສະເລ່ຍຂອງທາດປະສົມແລະຄູນຄ່ານີ້. ດ້ວຍ ຈຳ ນວນມະຫາຊົນຂອງໂມມູນຄົງທີ່, '' ຈາກນັ້ນ '' ຈະທະວີຄູນຜະລິດຕະພັນທີ່ທ່ານຫາພຽງແຕ່ 2.
- ກັບ H2: 1,007 x 2 = 2,014 ກຼາມຕໍ່ກ້ອນ; ສຳ ລັບ O2: 15,9994 x 2 = 31,9988 ກຼາມຕໍ່ກ້ອນ; ແລະ Cl2: 35,453 x 2 = 70,096 ກຣາມຕໍ່ເມັດ.
ວິທີທີ່ 2 ຂອງ 2: ຄຳ ນວນມະຫາຊົນໂມເລກຸນຂອງສານປະສົມ

ກຳ ນົດສູດໂຄງສ້າງຂອງສານປະສົມ. ສູດໂຄງສ້າງຂອງສານເຮັດໃຫ້ຕົວເລກປະລໍາມະນູຂອງແຕ່ລະອົງປະກອບທີ່ປະກອບເປັນທາດປະສົມນັ້ນ. (ຂໍ້ມູນນີ້ມີຢູ່ໃນປື້ມທີ່ອ້າງອີງທັງ ໝົດ). ຍົກຕົວຢ່າງ, ສູດສານເຄມີຂອງກົດ hydrochloric ແມ່ນ HCl; ຂອງ glucose ແມ່ນ C6ຮ12ອ6. ດ້ວຍສູດໂຄງສ້າງນີ້, ພວກເຮົາສາມາດ ກຳ ນົດ ຈຳ ນວນຂອງອະຕອມຂອງແຕ່ລະປະເພດທີ່ປະກອບທາດປະສົມທີ່ ກຳ ລັງພິຈາລະນາ.- ບ່ອນທີ່ HCl ມີປະລໍາມະນູໄຮໂດຼລິກ ໜຶ່ງ ແລະປະລໍາມະນູ chlorine 1 ໜ່ວຍ.
- ໂມເລກຸນທາດນ້ ຳ ຕານ C6ຮ12ອ6 ມີປະລໍາມະນູກາກບອນ 6, ປະລໍາມະນູ hydrogen 12 ແລະປະລໍາມະນູ oxygen 6.
ກຳ ນົດປະລິມານມວນສານສະເລ່ຍຂອງແຕ່ລະອົງປະກອບທີ່ປະກອບ. ໃຊ້ຕາຕະລາງແຕ່ລະໄລຍະເພື່ອຊອກຫາປະລິມານມະຫາສານສະເລ່ຍຂອງແຕ່ລະອົງປະກອບທີ່ປະກົດຢູ່ໃນສານປະສົມ. ອະຕອມຂອງມວນສານສະເລ່ຍແມ່ນຂຽນຕາມຮູບສັນຍາລັກທາງເຄມີຂອງອົງປະກອບໃນຕາຕະລາງແຕ່ລະໄລຍະ. ຄ້າຍຄືກັບການຄິດໄລ່ມວນສານໂມໂມຂອງອົງປະກອບໃດ ໜຶ່ງ, ຄູນປະລິມານມະຫາຊົນສະເລ່ຍໂດຍ 1 ກຣາມ / ມມ.
- ປະລິມານມະຫາຊົນສະເລ່ຍຂອງອົງປະກອບທີ່ປະກອບເປັນກົດ hydrochloric ມີດັ່ງນີ້: hydrogen 1,007 g / mol ແລະ chlorine 35,453 g / mol.
- ປະລິມານມະຫາຊົນສະເລ່ຍຂອງອົງປະກອບທີ່ປະກອບເປັນໂມເລກຸນ glucose ແມ່ນ: ຄາບອນ, 12,017 g / mol; hydrogen, 1,007 g / mol; ແລະອົກຊີເຈນ, 15,995 g / mol.
ຄິດໄລ່ມວນສານໂມໂມຂອງແຕ່ລະອົງປະກອບ. ປະສົມປະສານມວນສານຂອງທາດອົງປະກອບຕາມ ຈຳ ນວນອະຕອມທີ່ມັນປະກອບສ່ວນໃນທາດປະສົມເຮັດໃຫ້ມວນສານສະເລ່ຍຂອງທາດໃນທາດປະສົມ.
- ໃນກໍລະນີຂອງກົດ hydrochloric, ອາຊິດ hydrochloric, ມະຫາຊົນໂມ້ຂອງທາດອົງປະກອບ hydrogen ແມ່ນ 1,007 g / mol, ແລະຂອງ chlorine ແມ່ນ 35,453 g / mol.
- ໃນກໍລະນີຂອງນ້ ຳ ຕານ, C6ຮ12ອ6, ມະຫາຊົນມຸກຂອງແຕ່ລະອົງປະກອບມີດັ່ງນີ້: ກາກບອນ, 12.0107 x 6 = 72,0642 g / mol; hydrogen, 1,007 x 12 = 12,084 g / mol; ອົກຊີເຈນ, 15,9995 x 6 = 95,9964 g / mol.
ຈຳ ນວນມະຫາສານໂມ້ຂອງອົງປະກອບທີ່ປະກອບ. ມະຫາຊົນມຸກທັງ ໝົດ ຂອງອົງປະກອບຂອງການຍ່ອຍສະຫຼາຍແມ່ນມະຫາຊົນໂມລາຂອງທາດປະສົມ.ໃນບາດກ້າວທີ່ຜ່ານມາພວກເຮົາໄດ້ຄິດໄລ່ມວນສານໂມໂມຂອງແຕ່ລະອົງປະກອບທີ່ມີຢູ່ໃນສານປະສົມ, ໃນຂັ້ນຕອນນີ້ພວກເຮົາພຽງແຕ່ຕ້ອງການເພີ່ມຄ່າທັງ ໝົດ ນີ້ເຂົ້າກັນ.
- ມະຫາຊົນ Molar ຂອງກົດ hydrochloric ແມ່ນ 1,007 + 35,453 = 36,460 g / mol. ຂະ ໜາດ 36,46 ກຣາມແມ່ນມວນສານຂອງອາຊິດ hydrochloric 1 mol.
- ມະຫາຊົນຂອງນ້ ຳ ຕານແມ່ນ 72,0642 + 12,084 + 95,9964 = 180,1446 g / mol. ສະນັ້ນແຕ່ລະມົມຂອງນ້ ຳ ຕານໃນນ້ ຳ ໜັກ ມີ 180,14 ກຣາມ.
ຄຳ ແນະ ນຳ
- ເຖິງແມ່ນວ່າໃນກໍລະນີຫຼາຍທີ່ສຸດ, ປະລິມານມະຫາຊົນສະເລ່ຍໄດ້ຖືກບັນທຶກເປັນ 1 ສ່ວນທີ່ໃກ້ທີ່ສຸດ 1000 (ສະຖານທີ່ 4 ທົດສະນິຍົມ), ໃນຫ້ອງທົດລອງ, ມະຫາຊົນໂມມົມມັກຈະຖືກຫຼຸດລົງເປັນ 2 ສະຖານທີ່ທົດສະນິຍົມ, ບາງຄັ້ງກໍ່ ໜ້ອຍ ກວ່າ, ສຳ ລັບໂມເລກຸນຂະ ໜາດ ໃຫຍ່. ດັ່ງນັ້ນ, ໃນກໍລະນີໃນຫ້ອງທົດລອງ, ສານມະຫາຊົນຂອງທາດໂມໄຊກຼາມອາດຈະຖືກຂຽນເປັນ 36,46 ກຣາມຕໍ່ລິດ, ສຳ ລັບນ້ ຳ ຕານ 180,14 ກຼາມຕໍ່ 1 ມມ.
ເຈົ້າຕ້ອງການຫັຍງ
- ປື້ມອ້າງອີງທາງເຄມີຫຼືຕາຕະລາງແຕ່ລະໄລຍະຂອງອົງປະກອບ
- ຄອມພິວເຕີ