ກະວີ:
Randy Alexander
ວັນທີຂອງການສ້າງ:
1 ເດືອນເມສາ 2021
ວັນທີປັບປຸງ:
1 ເດືອນກໍລະກົດ 2024
ເນື້ອຫາ
ໃນເຄມີສາດ, ເອເລັກໂຕຣນິກ valence ແມ່ນເອເລັກໂຕຣນິກຕັ້ງຢູ່ຊັ້ນນອກຂອງຫອຍເອເລັກໂຕຣນິກຂອງອົງປະກອບໃດ ໜຶ່ງ. ການ ກຳ ນົດ ຈຳ ນວນເອເລັກໂຕຣນິກທີ່ມີຄຸນຄ່າຂອງອົງປະກອບໃດ ໜຶ່ງ ແມ່ນທັກສະທີ່ ສຳ ຄັນໃນເຄມີສາດເພາະວ່າຂໍ້ມູນນີ້ຈະຊ່ວຍໃນການ ກຳ ນົດຊະນິດພັນທະບັດທີ່ອົງປະກອບສາມາດປະກອບຂື້ນມາ. ການ ກຳ ນົດ ຈຳ ນວນເອເລັກໂຕຣນິກທີ່ມີຄຸນຄ່າສາມາດເຮັດໄດ້ງ່າຍດ້ວຍຕາຕະລາງແຕ່ລະໄລຍະຂອງອົງປະກອບເຄມີ.
ຂັ້ນຕອນ
ສ່ວນທີ 1 ຂອງ 2: ຊອກຫາ ຈຳ ນວນຂອງເອເລັກໂຕຣນິກ valence ໂດຍ ນຳ ໃຊ້ຕາຕະລາງແຕ່ລະໄລຍະ
ດ້ວຍໂລຫະທີ່ບໍ່ປ່ຽນແປງ
ກຽມພ້ອມແລ້ວ ຕາຕະລາງແຕ່ລະໄລຍະ ທາດເຄມີ. ຕາຕະລາງແຕ່ລະໄລຍະຂອງອົງປະກອບ (ຕາຕະລາງແຕ່ລະໄລຍະ ສຳ ລັບສັ້ນ) ແມ່ນຕາຕະລາງຫຼາຍຫ້ອງທີ່ມີລະຫັດສີເຊິ່ງມີລາຍຊື່ທຸກໆອົງປະກອບທີ່ຮູ້ຈັກພ້ອມທັງຂໍ້ມູນທີ່ ຈຳ ເປັນບາງຢ່າງກ່ຽວກັບ ອົງປະກອບເຫຼົ່ານັ້ນ. ອີງຕາມຂໍ້ມູນທີ່ມີຢູ່ໃນຕາຕະລາງແຕ່ລະໄລຍະ, ພວກເຮົາສາມາດ ກຳ ນົດ ຈຳ ນວນເອເລັກໂຕຣນິກທີ່ມີຄຸນຄ່າຂອງອົງປະກອບທີ່ພວກເຮົາ ກຳ ລັງສືບສວນ. ຕາຕະລາງແຕ່ລະໄລຍະແມ່ນຕິດກັບປື້ມ ຕຳ ລາຮຽນ. ທ່ານຍັງສາມາດອ້າງອີງຕາຕະລາງໄລຍະເວລາແບບໂຕ້ຕອບທີ່ມີຢູ່ນີ້.

ໝາຍ ເລກແຕ່ລະຖັນໃນຕາຕະລາງແຕ່ລະໄລຍະແຕ່ວັນທີ 1 ເຖິງ 18. ໂດຍປົກກະຕິຢູ່ໃນຕາຕະລາງແຕ່ລະໄລຍະ, ທຸກໆອົງປະກອບທີ່ຢູ່ໃນຖັນດຽວກັນຈະມີ ຈຳ ນວນເອເລັກໂຕຣນິກ valence ດຽວກັນ. ຖ້າຕາຕະລາງແຕ່ລະໄລຍະຂອງທ່ານຍັງບໍ່ໄດ້ນັບ ຈຳ ນວນຖັນ, ກະລຸນາເຮັດດ້ວຍຕົວເອງໂດຍການ ໝາຍ ເລກ 1 ເຖິງ 18 ຕັ້ງແຕ່ຊ້າຍຫາຂວາ. ທາງດ້ານວິທະຍາສາດ, ແຕ່ລະຖັນໃນຕາຕະລາງແຕ່ລະໄລຍະຖືກເອີ້ນວ່າ ໜຶ່ງ "ກຸ່ມ".- ຍົກຕົວຢ່າງ, ສຳ ລັບຕາຕະລາງໄລຍະເວລາທີ່ບໍ່ໄດ້ລົງນາມ, ພວກເຮົາຈະ ໝາຍ ເລກ 1 ສູງກວ່າທາດໄຮໂດເຈນ (H), ເລກທີ 2 ຢູ່ ເໜືອ ທາດ Beri (Be) ແລະເຮັດເຊັ່ນດຽວກັນຈົນຮອດ 18 ເໜືອ Helium (ລາວ) ).

ກຳ ນົດ ຕຳ ແໜ່ງ ຂອງອົງປະກອບໃນ ຄຳ ຖາມ. ໃນຂັ້ນຕອນນີ້ ກຳ ນົດ ຕຳ ແໜ່ງ ຂອງອົງປະກອບທີ່ທ່ານ ກຳ ລັງເບິ່ງຢູ່ໃນຕາຕະລາງແຕ່ລະໄລຍະ. ທ່ານສາມາດຊອກຫາ ຕຳ ແໜ່ງ ຂອງອົງປະກອບໂດຍອີງໃສ່ສັນຍາລັກທາງເຄມີຂອງມັນ (ຈົດ ໝາຍ ໃນແຕ່ລະຫ້ອງ), ເລກປະລໍາມະນູ (ຕົວເລກຢູ່ແຈເບື້ອງຊ້າຍດ້ານເທິງຂອງແຕ່ລະຫ້ອງ), ຫຼືອີງໃສ່ຂໍ້ມູນ ຂໍ້ຄວາມມີຢູ່ໃນຕາຕະລາງແຕ່ລະໄລຍະ.- ຕົວຢ່າງພວກເຮົາ ຈຳ ເປັນຕ້ອງຊອກຫາ ຈຳ ນວນຂອງເອເລັກໂຕຣນິກ valence ຂອງອົງປະກອບ ກາກບອນ (C). ຕົວເລກປະລໍາມະນູຂອງອົງປະກອບແມ່ນ 6. ຄາບອນແມ່ນຢູ່ໃນສ່ວນເທິງຂອງກຸ່ມ 14 ສ່ວນໃນຂັ້ນຕອນຕໍ່ໄປພວກເຮົາຈະ ກຳ ນົດ ຈຳ ນວນຂອງເອເລັກໂຕຣນິກ valence ຂອງອົງປະກອບນີ້.
- ໃນພາກນີ້ພວກເຮົາຈະບໍ່ສົນໃຈໂລຫະ Transition, ເຊັ່ນ: ອົງປະກອບຕ່າງໆໃນຂອບເຂດຂອງກຸ່ມ 3 ເຖິງ 12. ໂລຫະຫັນປ່ຽນເຫຼົ່ານີ້ແຕກຕ່າງຈາກສ່ວນທີ່ເຫຼືອ, ສະນັ້ນຂັ້ນຕອນແມ່ນ ຄຳ ແນະ ນຳ ທີ່ໃຫ້ໄວ້ໃນພາກນີ້ບໍ່ໄດ້ ນຳ ໃຊ້ກັບໂລຫະປະເພດນີ້. ພວກເຮົາຈະເບິ່ງກຸ່ມຂອງອົງປະກອບເຫຼົ່ານີ້ຕໍ່ມາໃນບົດຄວາມ.

ໃຊ້ຕົວເລກກຸ່ມເພື່ອ ກຳ ນົດ ຈຳ ນວນຂອງເອເລັກໂຕຣນິກ valence. ເລກກຸ່ມຂອງໂລຫະທີ່ບໍ່ປ່ຽນແປງສາມາດຖືກ ນຳ ໃຊ້ເພື່ອຄິດໄລ່ ຈຳ ນວນເອເລັກໂຕຣນິກທີ່ມີຄຸນຄ່າໃນອະຕອມຂອງອົງປະກອບນັ້ນ. "ແຖວແຖວຂອງ ຈຳ ນວນກຸ່ມ" ແມ່ນ ຈຳ ນວນເອເລັກໂຕຣນິກທີ່ມີຄ່າໃນອະຕອມຂອງອົງປະກອບໃນກຸ່ມນັ້ນ. ໃນຄໍາສັບຕ່າງໆອື່ນໆ:- ກຸ່ມທີ 1: ເອເລັກໂຕຣນິກ valence 1
- ກຸ່ມ 2: ເອເລັກໂຕຣນິກ valence 2
- ກຸ່ມ 13: 3 ເອເລັກໂຕຣນິກ valence
- ກຸ່ມ 14: 4 ເອເລັກໂຕຣນິກ valence
- ກຸ່ມ 15: 5 ເອເລັກໂຕຣນິກ valence
- ກຸ່ມ 16: 6 ເອເລັກໂຕຣນິກ valence
- ກຸ່ມ 17: 7 ເອເລັກໂຕຣນິກ valence
- ກຸ່ມ 18: 8 ເອເລັກໂຕຣນິກ valence (ຍົກເວັ້ນເຮເລຍດ້ວຍໄຟຟ້າ valence 2)
- ໃນຕົວຢ່າງກາກບອນ, ເນື່ອງຈາກກາກບອນຢູ່ໃນກຸ່ມ 14, ພວກເຮົາສາມາດເວົ້າໄດ້ວ່າອະຕອມຄາບອນມີ ສີ່ເອເລັກໂຕຣນິກ valence.
ດ້ວຍໂລຫະການຫັນປ່ຽນ
ກຳ ນົດອົງປະກອບໃດ ໜຶ່ງ ໃນຂອບເຂດຕັ້ງແຕ່ກຸ່ມ 3 ເຖິງກຸ່ມ 12. ດັ່ງທີ່ໄດ້ກ່າວມາຂ້າງເທິງ, ອົງປະກອບທີ່ຢູ່ໃນກຸ່ມ 3 ເຖິງ 12 ຖືກເອີ້ນວ່າ "ໂລຫະການປ່ຽນແປງ" ແລະເມື່ອເວົ້າເຖິງຄວາມມີຄ່າໄຟຟ້າເອເລັກໂຕຣນິກເຫຼົ່ານີ້ມີຄຸນສົມບັດທີ່ແຕກຕ່າງຈາກສ່ວນທີ່ເຫຼືອ. ໃນພາກນີ້, ພວກເຮົາຈະຮຽນຮູ້ວ່າເປັນຫຍັງສ່ວນຫຼາຍແລ້ວມັນບໍ່ເປັນໄປໄດ້ທີ່ຈະມອບຄ່າເອເລັກໂຕຣນິກທີ່ມີຄຸນຄ່າໃຫ້ກັບອະຕອມຂອງໂລຫະການຫັນປ່ຽນ.
- ໃນພາກນີ້ພວກເຮົາເອົາສ່ວນປະກອບທີ່ວ່າ Tantan (Ta) ເຊິ່ງຕົວເລກປະລໍາມະນູຂອງມັນແມ່ນ 73 ເປັນຕົວຢ່າງ. ຂັ້ນຕອນຕໍ່ໄປຈະຊ່ວຍໃນການ ກຳ ນົດ ຈຳ ນວນຂອງອິເລັກໂທຣນິກທີ່ມີຄ່າ.
- ໃຫ້ສັງເກດວ່າອົງປະກອບຂອງ 3 ຕະກຽງ lantans ແລະ actinium (ທີ່ເອີ້ນວ່າ "ໂລຫະແຜ່ນດິນໂລກທີ່ຫາຍາກ") ຍັງຂຶ້ນກັບກຸ່ມຂອງໂລຫະການຫັນປ່ຽນ - ສອງອົງປະກອບຂອງອົງປະກອບນີ້ມັກຈະມີລາຍຊື່ຢູ່ລຸ່ມຕາຕະລາງແຕ່ລະໄລຍະ. ຫົວກັບ lantan ແລະ actini.
ເອເລັກໂຕຣນິກທີ່ມີຄຸນຄ່າໃນໂລຫະການປ່ຽນແປງບໍ່ຄືກັບ 'ປົກກະຕິ' valence ເອເລັກໂຕຣນິກ 'ປົກກະຕິ'. ເພື່ອເຂົ້າໃຈວ່າເປັນຫຍັງໂລຫະການຫັນປ່ຽນຕົວຈິງບໍ່ໄດ້ເຮັດວຽກ '' ຄືກັບອົງປະກອບອື່ນໆໃນຕາຕະລາງແຕ່ລະໄລຍະ, ພວກເຮົາຕ້ອງຮູ້ເລັກນ້ອຍກ່ຽວກັບວິທີເອເລັກໂຕຣນິກເຮັດວຽກໃນອະຕອມດັ່ງທີ່ໄດ້ອະທິບາຍຂ້າງລຸ່ມນີ້. , ຫຼືທ່ານສາມາດຂ້າມຂັ້ນຕອນນີ້.
- ເມື່ອເອເລັກໂຕຣນິກຖືກໃສ່ເຂົ້າໄປໃນອະຕອມ, ພວກມັນຖືກຈັດເຂົ້າໃນ "ວົງໂຄຈອນ" ທີ່ແຕກຕ່າງກັນ - ນັ້ນແມ່ນຂົງເຂດທີ່ແຕກຕ່າງກັນອ້ອມຮອບແກນ. ໃນຄວາມສັ້ນ, valence ເອເລັກໂຕຣນິກແມ່ນເອເລັກໂຕຣນິກທີ່ຕັ້ງຢູ່ໃນຊັ້ນນອກຂອງວົງໂຄຈອນ - ໃນຄໍາສັບຕ່າງໆອື່ນໆ, ເອເລັກໂຕຣນິກສຸດທ້າຍທີ່ເພີ່ມເຂົ້າໄປໃນປະລໍາມະນູ.
- ການອະທິບາຍວົງໂຄຈອນໃນລາຍລະອຽດອາດຈະເປັນເລື່ອງເລັກນ້ອຍ, ເມື່ອມີການເພີ່ມເອເລັກໂຕຣນິກເຂົ້າໃນ subclass ງ ຂອງຫອຍປະລໍາມະນູຂອງໂລຫະການຫັນປ່ຽນ (ເບິ່ງຂ້າງລຸ່ມນີ້), ທໍາອິດຂອງເອເລັກໂຕຣນິກເຫຼົ່ານີ້ຈະປະຕິບັດຄືກັບເອເລັກໂຕຣນິກ valence ປົກກະຕິ, ແຕ່ຕໍ່ມາຄຸນສົມບັດຂອງມັນສາມາດປ່ຽນແປງ, ເພີ່ມ ໃນເວລາທີ່ເອເລັກໂຕຣນິກຈາກວົງຈອນອື່ນໆສາມາດເຮັດຫນ້າທີ່ເປັນເອເລັກໂຕຣນິກ valence. ນັ້ນແມ່ນ, ປະລໍາມະນູສາມາດມີເອເລັກໂຕຣນິກ valence ຫຼາຍຂື້ນຢູ່ກັບກໍລະນີ.
- ທ່ານສາມາດຮຽນຮູ້ເພີ່ມເຕີມກ່ຽວກັບສິ່ງນີ້ໄດ້ທີ່ Clackamas Community College valence electron site.
ກຳ ນົດ ຈຳ ນວນເອເລັກໂຕຣນິກທີ່ມີຄ່າໂດຍອີງໃສ່ ຈຳ ນວນກຸ່ມ. ດັ່ງທີ່ໄດ້ລະບຸໄວ້ຂ້າງເທິງ ສຳ ລັບໂລຫະທີ່ບໍ່ປ່ຽນ, ຈຳ ນວນກຸ່ມໃນຕາຕະລາງແຕ່ລະໄລຍະສາມາດຊ່ວຍ ກຳ ນົດ ຈຳ ນວນຂອງເອເລັກໂຕຣນິກ valence. ເຖິງຢ່າງໃດກໍ່ຕາມ, ບໍ່ມີສູດທີ່ແນ່ນອນໃນການ ກຳ ນົດ ຈຳ ນວນທີ່ແນ່ນອນຂອງເອເລັກໂຕຣນິກທີ່ມີຄວາມ ສຳ ຄັນຂອງໂລຫະການປ່ຽນ - ໃນກໍລະນີນີ້ ຈຳ ນວນເອເລັກໂຕຣນິກທີ່ມີຄຸນຄ່າຂອງອົງປະກອບໃດ ໜຶ່ງ ແມ່ນບໍ່ມີມູນຄ່າຄົງທີ່, ຈຳ ນວນຂອງສິ່ງຕ່າງໆ. ກຸ່ມຕົນເອງພຽງແຕ່ສາມາດບອກ ຈຳ ນວນທີ່ກ່ຽວຂ້ອງຂອງເອເລັກໂຕຣນິກ valence. ລາຍລະອຽດ:
- ກຸ່ມທີ 3: ເອເລັກໂຕຣນິກ valence 3
- ກຸ່ມຂອງເອເລັກໂຕຣນິກ valence 4: 2 ຫາ 4
- ກຸ່ມທີ 5: 2 ຫາ 5 ຂອງເອເລັກໂຕຣນິກ valence
- ກຸ່ມທີ 6: ເອເລັກໂຕຣນິກ valence 2 ຫາ 2
- ກຸ່ມ 7: 2 ຫາ 7 ກັບເອເລັກໂຕຣນິກ valence
- ກຸ່ມຂອງເອເລັກໂຕຣນິກ valence 8: 2 ຫາ 3
- ກຸ່ມ 9: 2 ຫາ 3 ກັບເອເລັກໂຕຣນິກ valence
- ກຸ່ມຂອງ 10: 2 ຫາ 3 ເອເລັກໂຕຣນິກ valence
- ກຸ່ມ 11: 1 ເຖິງ 2 ເອເລັກໂຕຣນິກ valence
- ກຸ່ມ 12: 2 ເອເລັກໂຕຣນິກ valence
- ເອົາຕົວຢ່າງຂອງອົງປະກອບ Tanta (Ta) ຂອງກຸ່ມ 5, ພວກເຮົາສາມາດເວົ້າໄດ້ວ່າອົງປະກອບນີ້ມີ ຈາກ 2 ຫາ 5 ເອເລັກໂຕຣນິກ valence, ອີງຕາມກໍລະນີ.
ສ່ວນທີ 2 ຂອງ 2: ຊອກຫາ ຈຳ ນວນຂອງເອເລັກໂຕຣນິກ valence ໂດຍອີງໃສ່ການຕັ້ງຄ່າເອເລັກໂຕຣນິກ
ຮຽນຮູ້ວິທີການອ່ານການຕັ້ງຄ່າເອເລັກໂຕຣນິກ. ອີງຕາມການຕັ້ງຄ່າເອເລັກໂຕຣນິກຂອງອົງປະກອບໃດ ໜຶ່ງ, ພວກເຮົາຍັງສາມາດ ກຳ ນົດ ຈຳ ນວນເອເລັກໂຕຣນິກທີ່ມີຄຸນຄ່າຂອງອົງປະກອບນັ້ນ. ການຕັ້ງຄ່າເອເລັກໂຕຣນິກເບິ່ງຄືວ່າສັບສົນ, ແຕ່ວ່າມັນເປັນພຽງວິທີການທີ່ຈະເປັນຕົວແທນຂອງວົງໂຄຈອນຂອງອົງປະກອບໃນຮູບແບບຂອງຕົວອັກສອນແລະຕົວເລກ, ເມື່ອທ່ານໄດ້ກົດ ໝາຍ, ການເຂົ້າໃຈການຕັ້ງຄ່າເອເລັກໂຕຣນິກບໍ່ແມ່ນເລື່ອງຍາກ.
- ພິຈາລະນາຕົວຢ່າງການຕັ້ງຄ່າເອເລັກໂຕຣນິກຂອງ sodium (Na):
- 1s2s2p3s
- ຖ້າທ່ານເອົາໃຈໃສ່, ທ່ານຈະເຫັນວ່າການຕັ້ງຄ່າເອເລັກໂຕຣນິກແມ່ນພຽງແຕ່ສາຍຊ້ ຳ ອີກ:
- (number) (ຄຳ) (ຈຳ ນວນ) (ຄຳ) ...
- ... ແລະອື່ນໆ. ກຸ່ມ (ຈຳ ນວນ) (ຄຳ) ທຳ ອິດແມ່ນຊື່ຂອງວົງໂຄຈອນແລະ ໝາຍ ເຖິງ ຈຳ ນວນຂອງອິເລັກຕອນໃນວົງໂຄຈອນນັ້ນ.
- ດັ່ງນັ້ນ, ໃນກໍລະນີຂອງພວກເຮົາ, ພວກເຮົາສາມາດເວົ້າໄດ້ວ່າ sodium ເຮັດໄດ້ 2 ເອເລັກໂຕຣນິກໃນວົງໂຄຈອນ 1s, ເອເລັກໂຕຣນິກໃນວົງໂຄຈອນ 2s, 6 ເອເລັກໂຕຣນິກໃນວົງໂຄຈອນ 2p ແລະ 1 ເອເລັກໂຕຣນິກໃນ 3 3s ວົງໂຄຈອນ. ເອເລັກໂຕຣນິກທັງ ໝົດ 11 ຕົວ - ຕົວເລກປະລໍາມະນູຂອງໂຊດຽມແມ່ນ 11 ເຊັ່ນກັນ.
- ພິຈາລະນາຕົວຢ່າງການຕັ້ງຄ່າເອເລັກໂຕຣນິກຂອງ sodium (Na):
ຊອກຫາການຕັ້ງຄ່າເອເລັກໂຕຣນິກຂອງອົງປະກອບທີ່ທ່ານ ກຳ ລັງເບິ່ງຢູ່. ເມື່ອທ່ານຮູ້ການຕັ້ງຄ່າເອເລັກໂຕຣນິກຂອງອົງປະກອບ, ການຊອກຫາການຕັ້ງຄ່າເອເລັກໂຕຣນິກຂອງອົງປະກອບນັ້ນບໍ່ແມ່ນເລື່ອງຍາກ (ຍົກເວັ້ນໃນກໍລະນີຂອງໂລຫະການປ່ຽນແປງ). ຖ້າການຕັ້ງຄ່າເອເລັກໂຕຣນິກມີຢູ່ໃນ ຄຳ ຖາມທີ່ທ່ານຕ້ອງການແກ້ໄຂ, ທ່ານສາມາດຂ້າມຂັ້ນຕອນນີ້ໄດ້. ຖ້າທ່ານຕ້ອງການຊອກຫາການຕັ້ງຄ່າເອເລັກໂຕຣນິກ, ດຳ ເນີນຂັ້ນຕອນຕໍ່ໄປນີ້:
- ການຕັ້ງຄ່າເອເລັກໂຕຣນິກທີ່ສົມບູນຂອງອົງປະກອບ ununocti (Uuo), ຕົວເລກປະລໍາມະນູ 118 ແມ່ນ:
- 1s2s2p3s3p4s3d4p5s4d5p6s4f5d6p7s5f6d7p
- ເມື່ອທ່ານມີການຕັ້ງຄ່າເອເລັກໂຕຣນິກທີ່ສົມບູນແບບດັ່ງກ່າວ, ເພື່ອຊອກຫາການຕັ້ງຄ່າເອເລັກໂຕຣນິກຂອງອົງປະກອບອື່ນ, ທ່ານພຽງແຕ່ຕ້ອງການຕື່ມວົງໂຄຈອນກັບເອເລັກໂຕຣນິກ, ເລີ່ມຕົ້ນຈາກວົງໂຄຈອນ ທຳ ອິດ, ຈົນກ່ວາ ຈຳ ນວນເອເລັກໂຕຣນິກ ໝົດ ໄປເພື່ອຕື່ມ. ມັນຟັງເບິ່ງວ່າມັນສັບສົນ, ແຕ່ເມື່ອເວົ້າເຖິງການເຮັດມັນຂ້ອນຂ້າງງ່າຍ. ຕົວຢ່າງ: ຖ້າພວກເຮົາຕ້ອງການຂຽນການ ກຳ ນົດຄ່າເອເລັກໂຕຣນິກທີ່ສົມບູນຂອງ chlorine (Cl), ອົງປະກອບ 17, ນັ້ນແມ່ນ, ອະຕອມຂອງອົງປະກອບນີ້ມີ 17 ເອເລັກໂຕຣນິກ, ພວກເຮົາຈະຕື່ມຂໍ້ມູນດັ່ງຕໍ່ໄປນີ້:
- 1s2s2p3s3p
- ໃຫ້ສັງເກດວ່າ ຈຳ ນວນເອເລັກໂຕຣນິກທັງ ໝົດ ໃນການຕັ້ງຄ່າເອເລັກໂຕຣນິກແມ່ນຖືກຕ້ອງພຽງແຕ່ 17: 2 + 2 + 6 + 2 + 5 = 17. ທ່ານພຽງແຕ່ຕ້ອງການປ່ຽນຕົວເລກໃນວົງໂຄຈອນສຸດທ້າຍ - ສ່ວນທີ່ເຫຼືອຍັງຄົງຄືເກົ່າເພາະວ່າວົງໂຄຈອນໃກ້ຈະເຕັມແລ້ວ. ເອເລັກໂຕຣນິກ.
- ຮຽນຮູ້ເພີ່ມເຕີມກ່ຽວກັບວິທີການຂຽນການຕັ້ງຄ່າເອເລັກໂຕຣນິກຂອງອົງປະກອບ.
- ການຕັ້ງຄ່າເອເລັກໂຕຣນິກທີ່ສົມບູນຂອງອົງປະກອບ ununocti (Uuo), ຕົວເລກປະລໍາມະນູ 118 ແມ່ນ:

ມອບ ໝາຍ ເອເລັກໂຕຣນິກໃຫ້ກັບວົງໂຄຈອນຕາມກົດເກນທີແປດ. ເມື່ອເອເລັກໂຕຣນິກຖືກເພີ່ມເຂົ້າໄປໃນອະຕອມ, ພວກມັນຖືກຈັດເຂົ້າໃນວົງໂຄຈອນຕາມ ລຳ ດັບທີ່ໄດ້ລະບຸໄວ້ຂ້າງເທິງ - ສອງເອເລັກໂຕຣນິກ ທຳ ອິດຈະຖືກວາງຢູ່ໃນວົງໂຄຈອນ 1s, ສອງເອເລັກໂຕຣນິກຕໍ່ໄປໃນວົງໂຄຈອນ 2s, ອີກຫົກເອເລັກໂຕຣນິກຕໍ່ໄປຖືກວາງຢູ່ໃນວົງໂຄຈອນ 2p, ເຮັດແນວນັ້ນຈົນກ່ວາເອເລັກໂຕຣນິກຖືກຈັດໃສ່ໃນວົງໂຄຈອນທີ່ສອດຄ້ອງກັນ. ເມື່ອພວກເຮົາພິຈາລະນາອະຕອມຂອງອົງປະກອບທີ່ບໍ່ປ່ຽນແປງ, ພວກເຮົາສາມາດເວົ້າໄດ້ວ່າວົງໂຄຈອນເຫຼົ່ານີ້ຈະປະກອບເປັນ "ຊັ້ນ" ອ້ອມຮອບແກນ, ໃນນັ້ນຊັ້ນດ້ານຫຼັງຈະຢູ່ຫ່າງໄກຈາກ nucleus ຫຼາຍກ່ວາ ໜຶ່ງ ກ່ອນມັນ. ນອກ ເໜືອ ຈາກຊັ້ນ ທຳ ອິດທີ່ສາມາດຈັບໄດ້ພຽງແຕ່ສອງເອເລັກໂຕຣນິກ, ທຸກຊັ້ນຂອງວົງໂຄຈອນທີ່ຕິດຕໍ່ກັນສາມາດບັນຈຸເອເລັກໂຕຣນິກໄດ້ເຖິງແປດ (ຍົກເວັ້ນໃນກໍລະນີຂອງໂລຫະປ່ຽນ). ກົດລະບຽບນີ້ເອີ້ນວ່າ ກົດເກນສິບແປດ.- ຍົກຕົວຢ່າງ, ພິຈາລະນາອົງປະກອບ Bo (B). ຕົວເລກປະລໍາມະນູຂອງອົງປະກອບນີ້ແມ່ນ 5, ດັ່ງນັ້ນພວກເຮົາມີການຕັ້ງຄ່າເອເລັກໂຕຣນິກຂອງອົງປະກອບນີ້ຄືດັ່ງຕໍ່ໄປນີ້: 1s2s2p. ເນື່ອງຈາກວ່າຫອຍໂຄນ ໜ່ວຍ ທຳ ອິດມີພຽງແຕ່ສອງເອເລັກໂຕຣນິກ, ສາມາດ ກຳ ນົດໄດ້ວ່າ Bo ມີສອງຊັ້ນໃນວົງໂຄຈອນ: ໜ່ວຍ ທີ ໜຶ່ງ ປະກອບມີ 2 ເອເລັກໂຕຣນິກຢູ່ທີ່ວົງໂຄຈອນ 1s ແລະ ໜ່ວຍ ທີສອງມີສາມເອເລັກໂຕຣນິກແຈກຢາຍຢູ່ໃນວົງໂຄຈອນ 2s ແລະ 2p. .
- ສຳ ລັບຕົວຢ່າງອື່ນ, ອົງປະກອບທີ່ຄ້າຍຄືກັນກັບ chlorine ຈະມີ 3 ຊັ້ນ: ຊັ້ນຂອງອິເລັກຕອນໃນ 1 orbital, ຊັ້ນຂອງສອງອິເລັກຕອນໃນວົງໂຄຈອນ 2s ແລະຫົກເອເລັກໂຕຣນິກໃນວົງໂຄຈອນ 2p, ແລະຊັ້ນນອກຂອງສອງອິເລັກຕອນໃນວົງໂຄຈອນ 3. ແລະຫ້າເອເລັກໂຕຣນິກໃນວົງໂຄຈອນ 3p.
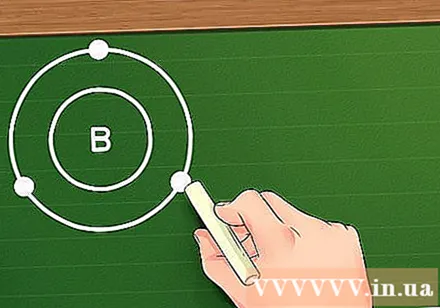
ຊອກຫາ ຈຳ ນວນເອເລັກໂຕຣນິກໃນຊັ້ນນອກ. ເມື່ອການ ກຳ ນົດຄ່າເອເລັກໂຕຣນິກໄດ້ຖືກ ກຳ ນົດແລ້ວ, ພວກເຮົາຮູ້ຈັກຊັ້ນຂອງອົງປະກອບນັ້ນແລ້ວ, ການຄົ້ນຫາ ຈຳ ນວນຂອງເອເລັກໂຕຣນິກທີ່ມີຄວາມສາມາດເຮັດໄດ້ໂດຍການ ກຳ ນົດ ຈຳ ນວນເອເລັກໂຕຣນິກໃນຊັ້ນນອກຂອງຫອຍເອເລັກໂຕຣນິກ. ຖ້າຊັ້ນນອກແມ່ນເຕັມ ໝົດ (ເຊັ່ນວ່າມີເອເລັກໂຕຣນິກທັງ ໝົດ 8 ໜ່ວຍ, ຫຼື ສຳ ລັບເອເລັກໂຕຣນິກຊັ້ນ 2 2) ແລ້ວທາດນັ້ນເອີ້ນວ່າອົງປະກອບທີ່ບໍ່ມີປະສິດຕິພາບແລະມີສ່ວນກ່ຽວຂ້ອງກັບທາດປະຕິກິລິຍາເຄມີ. ເຖິງຢ່າງໃດກໍ່ຕາມ, ກົດລະບຽບນີ້ບໍ່ໄດ້ ນຳ ໃຊ້ກັບໂລຫະການຫັນປ່ຽນ.- ຍົກຕົວຢ່າງ Bo, ເພາະວ່າ Bo ມີສາມເອເລັກໂຕຣນິກຢູ່ໃນຊັ້ນທີສອງ, ຍັງມີຊັ້ນນອກ, ດັ່ງນັ້ນພວກເຮົາສາມາດເວົ້າໄດ້ວ່າອົງປະກອບ Bo ມີ ພໍ່ ເອເລັກໂຕຣນິກ valence.

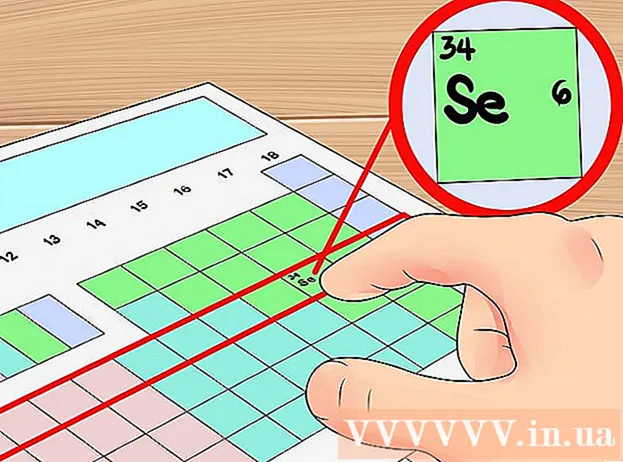
ໃຊ້ເລກແຖວໃນຕາຕະລາງແຕ່ລະໄລຍະເປັນວິທີທີ່ຫຍໍ້ເພື່ອ ກຳ ນົດ ຈຳ ນວນຊັ້ນຂອງວົງໂຄຈອນ. ແຖວຕາມແນວນອນໃນຕາຕະລາງແຕ່ລະໄລຍະຖືກເອີ້ນ "ວົງຈອນ" ຂອງອົງປະກອບ. ເລີ່ມຕົ້ນຈາກແຖວ ທຳ ອິດ, ແຕ່ລະຮອບຂອງວົງຈອນເທົ່າກັບ 'ຈຳ ນວນຊັ້ນອີເລັກໂທຣນິກ' ຂອງອົງປະກອບໃນໄລຍະດຽວກັນ. ດັ່ງນັ້ນ, ທ່ານສາມາດໃຊ້ໄລຍະເວລາເພື່ອ ກຳ ນົດ ຈຳ ນວນເອເລັກໂຕຣນິກທີ່ມີຄຸນຄ່າຂອງອົງປະກອບໃດ ໜຶ່ງ - ທ່ານພຽງແຕ່ນັບ ຈຳ ນວນເອເລັກໂຕຣນິກຕາມ ລຳ ດັບຈາກຊ້າຍຫາຂວາຈາກສ່ວນປະກອບ ທຳ ອິດຂອງໄລຍະນັ້ນ. ໃຫ້ສັງເກດອີກເທື່ອ ໜຶ່ງ ວ່າມັນບໍ່ສາມາດໃຊ້ກັບໂລຫະການປ່ຽນແປງ.- ຍົກຕົວຢ່າງ, ເນື່ອງຈາກວ່າເຊເລນຽມແມ່ນຢູ່ໃນວົງຈອນ 4, ມັນສາມາດຖືກ ກຳ ນົດວ່າອົງປະກອບມີສີ່ຊັ້ນເອເລັກໂຕຣນິກຢູ່ໃນຫອຍປະລໍາມະນູ. ເນື່ອງຈາກໃນ ຄຳ ສັ່ງຈາກຊ້າຍຫາຂວາ, ນີ້ແມ່ນອົງປະກອບທີ 6 ໃນວົງຈອນ 4 (ຍົກເວັ້ນໂລຫະການປ່ຽນແປງ), ພວກເຮົາສາມາດເວົ້າໄດ້ວ່າຫອຍຊີລີນທີສີ່ມີທາດເອເລັກໂຕຣນິກ 6 ໜ່ວຍ, ເຊັ່ນ: ອົງປະກອບນີ້ມີ ເອເລັກໂຕຣນິກ valence ຫົກ.
ຄຳ ແນະ ນຳ
- ໝາຍ ເຫດ, ການຕັ້ງຄ່າເອເລັກໂຕຣນິກສາມາດຂຽນສັ້ນໆໂດຍໃຊ້ທາດອາຍທີ່ຫາຍາກ (ອົງປະກອບຂອງກຸ່ມ 18) ແທນທີ່ຈະເປັນວົງໂຄຈອນຢູ່ເທິງສຸດຂອງການຕັ້ງຄ່າ. ຕົວຢ່າງ, ການຕັ້ງຄ່າເອເລັກໂຕຣນິກຂອງ sodium ສາມາດຂຽນເປັນ 3s1 - ນັ້ນແມ່ນການຕັ້ງຄ່າເອເລັກໂຕຣນິກຂອງ sodium ແມ່ນຄືກັນກັບຂອງ Neon ແຕ່ມີເອເລັກໂຕຣນິກພິເສດໃນວົງໂຄຈອນ 3s.
- ໂລຫະການປ່ຽນແປງອາດມີ subclasses valence ທີ່ບໍ່ຄົບຖ້ວນ. ເພື່ອ ກຳ ນົດ ຈຳ ນວນ valence ຂອງໂລຫະການຫັນປ່ຽນຢ່າງຖືກຕ້ອງ, ມັນ ຈຳ ເປັນຕ້ອງໄດ້ ນຳ ໃຊ້ຫຼັກການ quantum ທີ່ສັບສົນທີ່ບໍ່ໄດ້ຖືກ ກຳ ນົດໄວ້ໃນບົດຄວາມນີ້.
- ມັນຍັງມີຄວາມ ສຳ ຄັນທີ່ຈະຕ້ອງສັງເກດວ່າຕາຕະລາງແຕ່ລະໄລຍະຂອງທາດເຄມີສາມາດແຕກຕ່າງກັນໃນແຕ່ລະປະເທດ. ສະນັ້ນ, ໃຫ້ແນ່ໃຈວ່າທ່ານ ກຳ ລັງໃຊ້ຕາຕະລາງປະ ຈຳ ທີ່ໃຊ້ເວລາທົ່ວໄປທີ່ທ່ານອາໄສຢູ່ເພື່ອຫລີກລ້ຽງຄວາມສັບສົນ.
ເຈົ້າຕ້ອງການຫັຍງ
- ຕາຕະລາງແຕ່ລະໄລຍະຂອງອົງປະກອບເຄມີ
- ດິນສໍ
- ເຈ້ຍ